1、填空题 现有A、B、C、D、E、F原子序数依次增大的六种元素,且都位于周期表前四周期。A的单质是密度最小的气体,B的双原子单质分子中,σ键与π键数目之比为1:2;C与B形成的一种化合物在常温下呈红棕色,D单质与它同主族下一周期元素的单质组成的合金在常温下呈液态,可用作原子反应堆的导热剂。E与D位于同一周期,且E元素的单质、氧化物熔点都很高。化合物FA溶于B的最高价氧化物对应的水化物的稀溶液,能生成两种气体,溶液呈蓝色。
(1)D的离子结构示意图为____________;Q分子是B2C的等电子体,Q的结构简式为___________。
(2)基态F+的电子排布式为____________;BA3分子的立体结构为______________。
(3)BAs晶体所含化学键类型有______________;BAs与水反应的化学方程式为___________________。
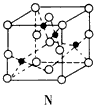
(4)如图是C、F元素组成的化合物M、N的晶胞示意图,M的化学式为_________,N的名称为_________。

参考答案:(1)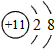 ;O=C=O
;O=C=O
(2)1s22s22p63s23p63d10;三角锥形
(3)离子键和极性共价键;NH4H+H2O=NH3・H2O+H2↑
(4)Cu2O;氧化铜
本题解析:
本题难度:一般
2、简答题 (I)CH3+、CH3-、CH3-都是重要的有机反应中间体,有关它们的说法正确的是______.
A.它们均由甲烷去掉一个氢原子所得
B.它们互为等电子体,碳原子均采取sp2杂化
C.CH3-与NH3、H3O+互为等电子体,几何构型均为三角锥形
D.CH3+中的碳原子采取sp2杂化,所有原子均共面
E.两个CH3-或一个CH3+和CH3-结合均可得到CH3CH3
(II)锌是一种重要的金属,锌及其化合物有着广泛的应用.
(1)指出锌在周期表中的位置:______周期,______族,______区.
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂.写出Zn2+基态电子排布式______;葡萄糖分子中碳原子杂化方式有______.
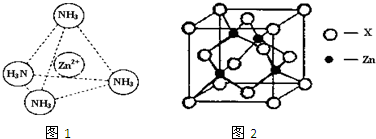
(3)Zn2+能与NH3形成配离子[Zn(NH3)4]2+.配位体NH3分子属于______(填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在图1中表示[Zn(NH3)4]2+中Zn2+与N之间的化学键.
(4)图2表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为______;该化合物的晶体熔点比干冰高得多,原因是______.
参考答案:(1)A.甲烷分子变成CH3+、CH3-、CH3-时,失去的分别是氢负离子、氢离子和质子,空间构型也不再与原来的分子相同,故A错误;
B.CH3+、CH3-、CH3-分别具有6个、7个和8个价电子,不是等电子体,中心碳原子的价层电子对数不同,故空间构型不同,故B错误;
C.CH3-与NH3、H3O+均具有10个电子,互为等电子体,几何构型均为三角锥形,故C正确;
D.CH3+中的碳原子采取sp2杂化,所有原子均共面,故D正确;
E.两个CH3-或一个CH3+和CH3-结合可得到CH3CH3,故E正确.
故选CDE.
(2)①Zn的原子序数是30,其电子排布式为:1s22s22p63s23p63d104s2,由电子排布式可知该元素为第四周期,第ⅡB族ds区,故答案为:四;ⅡB;ds;
②Zn2+基态电子排布式为:1s22s22p63s23p63d10或[Ar]3d10,葡萄糖里有两种碳原子,葡萄糖是无羟基醛,所以,一种是以sp3杂化(接羟基的碳),一种是以sp2杂化(醛基里的碳),故答案为:1s22s22p63s23p63d10或[Ar]3d10;sp2、sp3;
③配位体NH3分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,是极性分子;[Zn(NH3)4]2+中Zn2+与N之间的化学键是配位键,
故答案为:极性分子;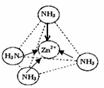 ;
;
④晶胞中锌的个数为4,X的个数为4,化学式为ZnX,该化合物是立体网状结构是原子晶体,而干冰是分子晶体,故该化合物的熔点比干冰高得多,
故答案为:ZnX;该化合物是原子晶体,而干冰是分子晶体.
本题解析:
本题难度:一般
3、填空题 (10分)某离子晶体的晶胞结构如图所示,试求:
(1)晶体中每一个Y同时吸引着______个X,每个X同时吸引着________个Y,该晶体的化学式是________。
(2)晶体中在每个X周围与它最接近且距离相等的X共有______个。
(3)设该晶体的摩尔质量为M g・mol-1,晶胞密度为ρ g・cm-3,阿伏加德罗常数为NA・mol-1,则晶体中两个最近的X中心间距离为________ cm。
参考答案:(1)4 8 XY2(或Y2X) (2)12 (3)
本题解析:(1)根据晶胞的结构可知,晶体中每一个Y同时吸引着4个X,每个X同时吸引着8个Y。因此该晶体的化学式为XY2(或Y2X)。
(2)晶体中在每个X周围与它最接近且距离相等的X位于面的面心处,共计是3×8÷2=12。
(3)设晶体中两个最近的X中心间距离为x,则晶胞的边长是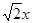 ,由于晶胞中含有4个X和8个Y,所以有
,由于晶胞中含有4个X和8个Y,所以有 ,解得x=
,解得x=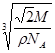 .
.
本题难度:一般
4、选择题 “拟晶”(quasicrystal)是一种具有凸多面体规则外形但不同于晶体的固态物质。A165Cu23Fel2是二十世纪发现的几百种拟晶之一,具有合金的某些优良物理性能。有关这种拟晶的说法错误的是:
A.A165Cu23Fel2的硬度比金属A1、Cu、Fe都大
B.A165Cu23Fel2中三种金属的化合价均可视作零
C.A165Cu23Fel2不可用作长期浸泡在海水中的材料
D.1mol A165Cu23Fel2溶于过量的硝酸时共失去265 mol电子
参考答案:D
本题解析:A、合金的硬度一般比各成分金属大,正确;B、Al65Cu23Fe12是由三种金属元素组成,由于金属无负价,根据化合价代数和为0的原则,三种金属的化合价均可视作零价,正确;C、A165Cu23Fel2长期浸泡在海水中易形成原电池,加快合金的腐蚀,故不可用作长期浸泡在海水中的材料,正确;D、A165Cu23Fel2溶于过量的硝酸时,Al与Fe均变为+3价,Cu变为+2价,故1 mol Al65Cu23Fe12失电子为277 mol,错误。
本题难度:一般
5、选择题 下列叙述中正确的是?(?)
A.阳离子不一定是金属离子,含阳离子的物质一定含阴离子
B.阴、阳离子相互作用不一定形成离子化合物
C.离子化合物均属于强电解质,都易溶于水
D.由某金属元素的阳离子和某非金属元素阴离子组成的物质一定是纯净物
参考答案:B
本题解析:略
本题难度:一般