1、选择题 下列实验操作能达到目的是( )
A.乙烷(乙烯),将混合气体通过盛有酸性KMnO4溶液的洗瓶,再用排气法收集
B.向蔗糖水解后的液体中加入新制Cu(OH)2悬浊液,加热到沸腾,验证水解产物为葡萄糖
C.通过灼烧的方法判断蚕织品和棉织品
D.用NaOH溶液除去CH3COOCH2CH3中少量CH3COOH
参考答案:C
本题解析:
本题难度:简单
2、选择题 下列根据实验操作和现象所得出的结论正确的是
选项
| 实验操作
| 实验现象
| 结论
|
A
| 向两份蛋白质溶液中分别滴加饱和NaCl 溶液和CuSO4溶液
| 均有固体析出
| 蛋白质均发生变性
|
B
| 向溶液X 中先滴加稀硝酸,再滴加Ba(NO3)2溶液
| 出现白色沉淀
| 溶液X 中一定含有SO42-
|
C
| 向一定浓度的Na2SiO3溶液中通入适量CO2气体
| 出现白色沉淀
| H2SiO3的酸性比H2CO3的酸性强
|
D
| 向浓度均为0. 1 mol・L-1 NaCl 和NaI 混合溶液中滴加少量AgNO3溶液
| 出现黄色沉淀
| Ksp(AgCl)>Ksp(AgI)
参考答案:D
本题解析:A项,蛋白质中加入NaCl发生盐析,加入CuSO4发生变性,错;B项,若原X中含有SO32-,加入稀HNO3,则会被氧化成SO42-,而与Ba2+生成沉淀,错;C项,反应方程式为:CO2+H2O+Na2SiO3 H2SiO3↓+ Na2CO3,该反应发生的原理为强酸制弱酸,即酸性:H2CO3>H2SiO3,错;D项,反应总是向着更难溶的方向进行,由于AgI的溶度积比AgCl小,所以优先生成AgI,正确。 H2SiO3↓+ Na2CO3,该反应发生的原理为强酸制弱酸,即酸性:H2CO3>H2SiO3,错;D项,反应总是向着更难溶的方向进行,由于AgI的溶度积比AgCl小,所以优先生成AgI,正确。
【考点定位】实验过程的现象及结论分析
本题难度:一般
3、填空题 (8分)有下列溶液①FeSO4、②MgCl2、③NH4NO3、④Na2SO4,分别加入A溶液可以将四种溶液鉴别出来。
(1)A可以是?溶液;将A溶液加入FeSO4溶液中,现象是___________________;
将A溶液加入MgCl2溶液中,现象是_________________________________。
(2)写出NH4NO3溶液加入A溶液加热反应的离子方程式 _______________________。
参考答案:(共8分,2分一空)(1)NaOH?生成白色沉淀,在空气中慢慢变成灰绿色,最终变红褐色;?生成白色沉淀?(2)NH4++OH-  NH3↑+H2O NH3↑+H2O
本题解析:(1)根据所给的物质的组成可知,利用氢氧化钠即可将其一一鉴别出来,所以A是氢氧化钠。氢氧化钠和硫酸亚铁反应的实验现象是生成白色沉淀,在空气中慢慢变成灰绿色,最终变红褐色。氢氧化镁能和氢氧化钠溶液反应生成氢氧化镁白色沉淀。
(2)硝酸铵能和氢氧化钠反应的离子方程式是NH4++OH-  NH3↑+H2O。 NH3↑+H2O。
点评:该题是高考中的常见考点,属于中等难度的试题,试题基础性强,侧重考查学生的能力。在进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。
本题难度:一般
4、填空题 某待测溶液(阳离子为Na+)中只可能含有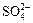 、 、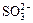 、Cl-、Br-、 、Cl-、Br-、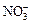 、 、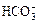 中的一种或若干种,进行下列实验(每次实验所加试剂均足量): 中的一种或若干种,进行下列实验(每次实验所加试剂均足量):
回答下列问题:
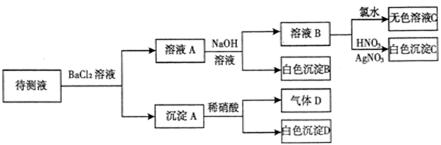
(1)待测液中是否含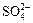 、 、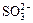 离子? 离子?
(2)气体D的化学式为?,反应生成沉淀B的离子方程式为:
?
(3)根据以上实验,待测液中肯定没有的离子?;肯定存在的离子是?。
参考答案:(1)一定有 SO32-,而 SO42- 可能存在可能不存在。
(2)NO,HCO3-+Ba2+ +OH- = BaCO3↓+H2O.
(3)Br-;HCO3-、SO32-
本题解析:略
本题难度:简单
5、选择题 用一种试剂鉴别乙醇、乙酸、乙醛、甲酸四种无色溶液,这种试剂是下列的? (? )
A.银氨溶液
B.浓氨水
C.FeCl3溶液
D.新制Cu(OH)2浊液
参考答案:D
本题解析:略
本题难度:简单
|