1、简答题 下列物质含有非极性共价键的共价化合物是( )
A.H2O2
B.HCl
C.Na2O2
D.Cl2
参考答案:A、H2O2既含有非极性共价键,又含有极性共价键,属于共价化合物,故A正确;
B、HCl为共价化合物,只含有性共价键,故B错误;
C、Na2O2既含有非极性共价键,又含有离子键,为离子化合物,故C错误;
D、Cl2为非金属单质,只含有非极性共价键,不属于化合物,故D错误.
故选A.
本题解析:
本题难度:一般
2、选择题 某稀有气体元素的原子序数为a,跟它的原子序数靠近的两种短周期元素X和Y相互化合时,能形成化学式为XY2的离子化合物.已知Y的原子序数为b,则X的原子序数为( )
A.a-b
B.2a-b
C.3a-2b
D.3b-2a
参考答案:C
本题解析:
本题难度:简单
3、选择题 下列表示物质结构的化学用语或模型正确的是( )
A.8个中子的氧原子的核素符号:
O
B.HF的电子式:
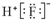
C.K+离子的结构示意图:
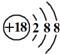
D.CH4分子的球棍模型:

参考答案:A
本题解析:
本题难度:一般
4、填空题 (15分)
已知:(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉作显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰。相关的反应如下:

4FeCl3+2NH2OH・HCl 4FeCl2+N2O↑+6HCl+H2O
4FeCl2+N2O↑+6HCl+H2O
①Fe2+在基态时,价层电子排布式 。 ②羟胺(NH2OH)中N原子的杂化方式 ?。
③Fe2+与邻啡罗啉形成的配合物中,配位数为 。
(2)硫酸铜晶体的化学式也可以表达为Cu(H2O)4SO4・H2O晶体,该晶体中含有的化学键类型是
(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、磷化镓及铜锢硒薄膜电池等。?其中元素P、As、Se第一电离能由小到大的顺序为: ?。
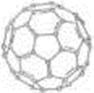

图1 ?图2
(4)① 有机太阳能固体电池材料含有高纯度C60,其结构如图1,则1 mol C60分子中π键的数目为 ,C60的晶胞结构如图2,则其配位数为_______若此晶胞的密度为ρg/cm3则两个最近C60间的距离为________cm(列式表达,已知阿伏伽德罗常数为NA)
② 如果把晶胞顶点与最近三个面心所围成的空隙叫做四面体空隙,第四周期电负性最小的原子可作为容体掺入C60晶体的空隙中,形成具有良好的超导性的掺杂C60化合物。若每个四面体空隙填入一个原子,则全部填满C60晶体的四面体空隙后,所形成的掺杂C60化合物的化学式为 。
参考答案:(1)①3d6;② sp3;③ 6;(2)离子键 共价键(配位键)
(3)Se< As< P?(4)① 30NA;12 ; ? ② K 2C60
? ② K 2C60
本题解析:(1)①Fe是26号元素,在Fe2+的核外有24个电子,在基态时,价层电子排布式3d6;②羟胺(NH2OH)中N原子的杂化方式sp3杂化; ③由化合物的结构简式可知:Fe2+与邻啡罗啉形成的配合物中,配位数为6;(2)在硫酸铜晶体Cu(H2O)4SO4・H2O中含有的化学键为离子键、共价键、配位键;(3)元素P、As是同一主族的元素,从上到下,原子半径增大,原子失去电子容易,所以第一电离能P>As;As、Se是同一周期的元素,原子半径As>Se,但是由于As原子的最外层的价电子处于该轨道的半充满的稳定状态,所以第一电离能As>Se.因此这三种元素的第一电离能由小到大的顺序为Se< As< P;(4)①在一个C60分子中含有60个C原子,每个C原子与连接的C原子形成了一个π键,而π键是两个原子所共有的,因此平均每个C原子含有的π键个数为1/2π键,。所以1 mol C60分子中π键的数目为60πNA÷2=30NA。由C60的晶胞结构示意图可知,它是立方面心结构,与每个C原子紧密连接的距离最近的C原子个数为(3÷8)÷2=12.即其配位数为12。每个晶胞中含有的C60分子个数是8×1/8+6×1/2=4;所以晶胞的边长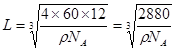 。根据晶胞示意图图可知两个最近C60间的距离为面对角线的一半,就是
。根据晶胞示意图图可知两个最近C60间的距离为面对角线的一半,就是 即为
即为 。②第四周期电负性最小的原子是K原子,由于每个顶点可形成1/4个四面体,一共有8个顶点,所以可形成2个正四面体。故可填充2个K原子,所形成的掺杂C60化合物的化学式为K 2C60。60化合物的化学式的确定的知识。
。②第四周期电负性最小的原子是K原子,由于每个顶点可形成1/4个四面体,一共有8个顶点,所以可形成2个正四面体。故可填充2个K原子,所形成的掺杂C60化合物的化学式为K 2C60。60化合物的化学式的确定的知识。
本题难度:一般
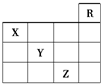
5、选择题 如图是元素周期表前四周期的一部分,下列对相关元素的叙述正确的是( )
①X元素的原子有二个电子层,处于周期表的第15个纵行 ②Z的原子序数为31,单质常温下为液体 ③气态氢化物水溶液的酸性X<Y<Z ④X的气态氢化物与Y的最高价氧化物的水化物能反应生成盐 ⑤Z的原子序数比Y大19,Y的原子序数比X大9.
A.只有②
B.只有①③④⑤
C.只有①②③④
D.全部