1、选择题 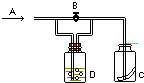 如图所示,A处通入Cl2,关闭B阀时,C处红色布条无变化;?打开B阀时,C处红色布条褪色,则D中的溶液是
如图所示,A处通入Cl2,关闭B阀时,C处红色布条无变化;?打开B阀时,C处红色布条褪色,则D中的溶液是
A.浓H2SO4
B.H2O
C.NaOH溶液
D.饱和食盐水
参考答案:AC
本题解析:分析:依据题干信息和发生的现象分析,干燥的氯气不能漂白有色布条,湿润的氯气能使有色布条褪色;
解答:A处通入Cl2,关闭B阀时,C处红色布条无变化;?打开B阀时,C处红色布条褪色,说明D装置的作用起到干燥氯气的作用,或吸收氯气,选项中的物质能干燥氯气的只有浓硫酸;能吸收氯气的是氢氧化钠溶液;
故选AC.
点评:本题考查了氯气的化学性质,干燥气体的试剂选择,装置图的理解和分析,注意氢氧化钠的吸收作用.
本题难度:一般
2、选择题 下列各组离子在指定溶液中可能大量共存的离子是
A.在强酸性溶液中:Mg2+、F-、Ba2+、NO3-
B.在pH=6的溶液中:K+、NO3-、Fe3+、Cl-
C.在NH4Cl溶液中:Ba2+、Na+、AlO2-、NO3-
D.使甲基橙变红的溶液中:Na+、NO3-、Al3+、SO42-
参考答案:D
本题解析:分析:A.F-与H+反应;
B.pH=6的溶液呈弱酸性,Fe3+不能大量存在;
C.NH4Cl溶液呈酸性;
D.使甲基橙变红的溶液呈酸性.
解答:A.强酸性溶液中F-与H+反应生成弱电解质,不能大量共存,故A错误;
B.Fe3+在pH约约为3.7时完全水解,则pH=6的溶液呈弱酸性,Fe3+不能大量存在,故B错误;
C.NH4+与AlO2-发生互促水解而不能大量共存,故C错误;
D.使甲基橙变红的溶液呈酸性,离子之间不发生任何反应,可大量共存,故D正确.
故选D.
点评:本题考查离子共存问题,综合考查元素化合物知识,侧重于考查学生化学知识的综合运用,易错点为B,注意铁离子水解的性质,题目难度不大.
本题难度:困难
3、选择题 某无色透明酸性溶液中,可以大量共存的离子组是
A.NH、NO、Al3+、Cl-
B.Fe2+、SO、NO、Na+
C.MnO、K+、SO、Na+
D.K+、SO、HCO、Na+
参考答案:A
本题解析:分析:酸性溶液中含大量的H+,根据离子之间不能结合生成水、气体、沉淀,不能发生氧化还原反应,则能大量共存,并结合离子的颜色李艾解答.
解答:A.酸性溶液中该组离子之间不反应,能大量共存,且均为无色,故A正确;
B.因Fe2+、NO3-、H+发生氧化还原反应,则不能共存,故B错误;
C.该组离子之间不反应,能共存,但MnO4-为紫色,与无色溶液不符,故C错误;
D.HCO3-、H+结合生成水和气体,则不能共存,故D错误;
故选A.
点评:本题考查离子的共存,熟悉复分解反应的条件及选项B中的氧化还原反应即可解答,题目难度不大,注意常见离子的颜色.
本题难度:简单
4、选择题 下列电离方程式的书写,正确的是
A.Ca(OH)2=Ca2++OH2-
B.FeSO4=Fe2++S6++4O2-
C.H2SO4=H++SO4-
D.NaHSO4=Na++H++SO42-
参考答案:D
本题解析:分析:强电解质可以完全电离,弱电解质部分电离,物质中的离子团不能拆开.
解答:A、氢氧化钙是强碱,能完全电离出钙离子和氢氧根离子,即Ca(OH)2=Ca2++2OH-,故A错误;
B、硫酸亚铁中的硫酸根不能拆开,应为:FeSO4=Fe2++SO42-,故B错误;
C、硫酸是强电解质,硫酸根带两个单位的负电荷,即H2SO4=2H++SO42-,故C错误;
D、NaHSO4在溶液中完全电离出三种离子,显强酸性,故D正确.
故选D.
点评:本题考查学生离子方程式的书写知识,可以根据所学知识进行回答,较简单.
本题难度:困难
5、选择题 下列离子方程式书写正确的是
A.氧化铝粉末投入NaOH溶液中:Al2O3+2OH-=2AlO2-+H2↑
B.金属钠与水反应:2Na+2H2O=2Na++2OH-+H2↑
C.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑
D.氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓
参考答案:B
本题解析:分析:A.从原子守恒角度考虑;
B.金属钠和水反应生成氢氧化钠和氢气;
C.碳酸钙是难溶物,不能拆成离子形式;
D.硫酸溶液跟氢氧化钡溶液反应生成硫酸钡沉淀和水.
解答:A、氧化铝是两性氧化物,既能和强酸反应又能和强碱反应,氧化铝粉末投入NaOH溶液中发生的反应为:
Al2O3+2OH-=2AlO2-+H2O,故A错误;
B、金属钠和水反应的实质是:2Na+2H2O=2Na++2OH-+H2↑,故B正确;
C、碳酸钙与盐酸反应的实质是:CaCO3+2H+=H2O+CO2↑+Ca2+,故C错误;
D、硫酸溶液跟氢氧化钡溶液反应生成硫酸钡沉淀和水,正确的离子方程式为:Ba2++2OH-+SO42-+2H+=2H2O↓+BaSO4↓,故D错误.
故选B.
点评:本题考查离子方程式的正误判断,题目难度中等,注意从守恒的角度判断离子方程式的正误,注意物质的性质以判断反应是否符合实际.
本题难度:一般