1、选择题 下列实验操作与实验目的相符的是( )
| 序号 | 实验操作
实验目的
A
测定HF、HCl的熔点、沸点
比较F、Cl的非金属性强弱
B
MgSO4、Al2(SO4)3溶液中分别滴加足量氨水
比较镁、铝的金属性强弱
C
将SO2气体通入碳酸钠溶液中
比较碳、硫的非金属性强弱
D
向氯化铵、氯化铝混合溶液中,滴加氢氧化钠溶液至过量
比较NaOH、NH3?H2O、Al(OH)3的碱性强弱
|
A.A
B.B
C.C
D.D
参考答案:A.HF、HCl的熔点、沸点属于物理性质,非金属性强弱属于化学性质,不能用物理性质来比较化学性质,故A错误;
B.MgSO4、Al2(SO4)3溶液中分别滴加足量氨水都生成沉淀,属于复分解反应,不能用来比较非金属性强弱,故B错误;
C.SO2气体通入碳酸钠溶液中先生成H2SO3,H2SO3的酸性比碳酸强,但比较非金属性应是最高价氧化物对应的水化物,故C错误;
D.向氯化铵、氯化铝混合溶液中,滴加氢氧化钠溶液至过量,符合强碱制取弱碱规律,NaOH碱性最强,如先生成沉淀说明氨水的碱性比氢氧化铝强,否则相反.故D正确.
故选D.
本题解析:
本题难度:简单
2、选择题 某主族元素的原子,M层上有一个半充满的能级,这种原子的质子数是 ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ?
A.只能是7
B.只能是15
C.是11或15
D.是11或13
参考答案:C
本题解析:正确答案:C
主族元素的原子,M层上有一个半充满的能级,可能是3s1或3s23p3,为Na或P, 质子数是11或15
本题难度:简单
3、填空题 A、B、C、D、E为短周期元素,A、B、C在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。D与A同周期,其最高正价与最低负价代数和为零。A、E可形成AE3型分子,分子中只存在极性键。

(1)B元素在元素周期表中的位置是_________________。
(2)C的离子结构示意图为_________________,用电子式表示AE3的形成过程:_________________。
(3)由元素A、C及氢元素形成的化合物中含有的化学键的类型有_________________。
(4)请设计一个实验来说明D与A的非金属性强弱(写出化学方程式即可)
__________________________________
参考答案:(1)第三周期VIA族
(2)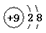 ;
;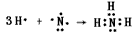
(3)离子键、极性共价键
(4)2HNO3+Na2CO3==2NaNO3+H2O+CO2↑
本题解析:
本题难度:一般
4、简答题 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑨九种元素在周期表中的位置.
族
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0
2
④
⑤
⑥
⑦
⑨
3
①
②
③
⑧
|
请回答:
(1)画出元素⑨的原子结构示意图______.
(2)九种元素中非金属性最强的是______(填元素符号).
(3)①、②两种元素原子半径比较:①______②(填“<”或“>”).在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是______(填化学式).
(4)⑦、⑧两种元素组成的氢化物的热稳定性比较:⑦______⑧(填“<”或“>”).
(5)元素⑤对应的氢化物的化学式是______,其水溶液的pH______7(填“<”或“>”).④、⑤两种元素对应的最高价含氧酸的酸性强的是______(填化学式).
(6)①、⑥两元素形成的化合物的电子式为______,该化合物是由______(填“共价键”“离子键”)键形成的.
参考答案:根据元素在周期表中的分布情况,可以确定①是Na,②是Mg,③是Al,④是C,⑤是N,⑥是O,⑦是F,⑧是Cl,⑨是Ne.
(1)Ne原子的结构示意图为:
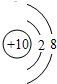
,故答案为:
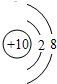
;
(2)同周期元素的原子从左到右非金属性逐渐增强,同一主族元素的原子从下到上非金属性逐渐增强,所以非金属性最强的元素在右上角,即为F,故答案为:F;
(3)根据元素周期律:同周期元素原子半径从左到右逐渐减小,所以原子半径Na>Mg,最高价氧化物对应水化物的碱性逐渐增强,所以碱性:NaOH>Mg(OH)2>Al(OH)3,
故答案为:>;?NaOH;
(4)根据元素周期律:同主族元素从上到下氢化物的稳定性逐渐减弱,所以稳定性HF>HCl,故答案为:>;
(5)元素N对应的氢化物的化学式是NH3,其水溶液氨水是弱碱,显碱性,它的pH>7,C、N两种元素对应的最高价含氧酸的酸性:硝酸>碳酸,故答案为:NH3;>;HNO3;
(6)Na、O两元素形成的化合物为氧化钠,氧化钠是氧离子和钠离子间通过离子键形成的离子化合物,它的电子式为

,
故答案为:

;离子.
本题解析:
本题难度:一般
5、选择题 下列有关物质性质比较的结论正确的是
A.碱性:NaOH>Mg(OH)2>Al(OH)3
B.碱性:Be(OH)2>LiOH
C.酸性:H2S>HCl
D.酸性:H2CO3>HNO3>H2SO4
参考答案:A
本题解析:
本题难度:简单