1��ѡ���� ������NH3ͨ��HNO3��AgNO3�Ļ����Һ�У����ɳ��������ʵ���(n)��ͨ��NH3�����(V)��ϵ(��ͼ��ʾ)��ȷ����(����)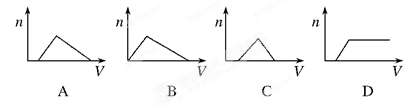
�ο��𰸣�A
����������Ⱥ�����������ӷ�Ӧ��
NH3��H��=NH4��? Ag����NH3��H2O=AgOH����NH4��? AgOH��2NH3��H2O=Ag(NH3)����OH����2H2O
�ɼ�ͼ��A��������
�����Ѷȣ���
2��ѡ���� ����NaBr ��KI�Ļ����Һ��ͨ�������Cl2��ַ�Ӧ������Һ���ɲ����գ����ʣ��Ĺ���������( ?)
A��NaCl ��KI
B��NaCl��KCl��I2
C��KCl��NaBr
D��KCl��NaCl
�ο��𰸣�D
�����������Cl2�������Դ���Br2��I2������Cl2�ܰ���Һ�е�B r�C��I�C������������Ӧ��2NaBr+Cl2=2NaCl+Br2��2KI+Cl2=2KCl+I2��ͨ�������Cl2����Һ�д���KCl��NaCl��Br2��I2����Br2�ӷ���ǿ��I2��������Ϊ���壬���Խ���Һ���ɲ����գ����ʣ�¹���������KCl��NaCl����ѡD��2�Ļӷ��Ժ�I2�����������ʡ�
�����Ѷȣ�һ��
3��ѡ���� ��a��b��c��d��e�������壬��������ʵ�飺
(1)a��b���
| ��������ɫ
|
(2)c��d���
| ��������
|
(3)c��e�ֱ�ͨ��������ˮ��
| ��ˮ�������ɫ����Һ��
|
(4)b��e�ֱ�ͨ����������
| ����������ɫ����
|
?
a��b��c��d��e�������(����)��
A��O2��NO��HCl��NH3��CO2
B��O2��NO��NH3��HCl��SO2
C��NO��O2��NH3��HCl��SO2
D��HCl��CO2��NH3��H2S��CH4
�ο��𰸣�C
���������a��b��Ϻ������ɺ���ɫ����֪a��b�ֱ�ΪNO��O2�е�һ�֣�bͨ���������в�������ɫ���ǣ���bΪO2��aΪNO��c��d��ϲ������̣���c��d�ֱ�ΪNH3��HCl�е�һ�֣�cͨ��������ˮ��ʹ��ˮ�����ɫ��Һ�壬��cΪNH3��dΪHCl��eͨ��������ˮ�У���ˮ�����ɫ����Һ�壬eͨ���������в�������ɫ���ǣ���eΪSO2��
�����Ѷȣ�һ��
4������� ��12�֣�A��B��C��D���������о�������Ԫ�ء�
�������µ���A��ij�ֳ���һԪǿ����Һ��Ӧ���ɵõ�B��C��B����ɫ��ӦΪ��ɫ��C��84����Һ����Ч�ɷ֡�
�ڻ�����D���ȴ��ֽ⣬���Ƶ�һ�����壬��������ʹ�����ǵ�ľ����ȼ��
(1)д��A��B��C��D�����ƣ�
A��_______________B��_______________C��_______________D��_______________
��2��д�����еĻ�ѧ��Ӧ����ʽ��_______________________________
��3��д�����еĻ�ѧ��Ӧ����ʽ��_______________________________
�ο��𰸣���12�֣� (1)A������? B���Ȼ���? C����������? D�������
��2��Cl2+2NaOH=NaCl+NaClO+H2O ��3��2KClO3 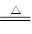 2KCl+3O2��
2KCl+3O2��
�����������1��B����ɫ��ӦΪ��ɫ��C��84����Һ����Ч�ɷ֣�����C�Ǵ������ƣ����A��������B���Ȼ��ơ�������D���ȴ��ֽ⣬���Ƶ�һ�����壬��������ʹ�����ǵ�ľ����ȼ������D������ء�
��2������������������Һ��Ӧ�ķ���ʽ��Cl2+2NaOH=NaCl+NaClO+H2O��
��3������طֽ�ķ���ʽ��2KClO3 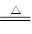 2KCl+3O2����
2KCl+3O2����
�����Ѷȣ�һ��
5��ѡ���� ���й����ȵ�˵����ȷ���� ?��?��
?��?��
A��Cl2��ʹ�ʻ���ɫ����ΪCl2����Ư����
B��Cl2���к�ǿ�������ԣ��ڻ�ѧ��Ӧ��ֻ����������
C����ˮ�����ֽ⣬������ˮӦ������ɫƿ�бܹⱣ��
D��ʵ���ҿ�����MnO2��ϡ���ᷴӦ�Ʊ�Cl2
�ο��𰸣�C
���������Cl2ʹ�ʻ���ɫ����ΪCl2���ʻ��е�ˮ��Ӧ���ɵ�HClO����Ư���ԣ�����������������Һ��Ӧʱ��������������������ԭ����MnO2��ϡ�����Ӧ�������Ʊ�Cl2Ӧ��Ũ���ᡣ
�����Ѷȣ���