1、选择题 用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.100mL1mol/LFeCl3溶液中含阳离子数为0.1NA
B.常温常压下1molNO2气体与水反应生成NA个NO3-离子
C.0.6gCaCO3与Mg3N2的混合物中所含质子数为0.3NA
D.80mL10mol/L浓盐酸与足量MnO2反应,转移电子数为0.4NA
参考答案:A、若铁离子不水解,100mL1mol/LFeCl3溶液中含阳离子数约为0.1L×1mol/L×NAmol-1=0.1NA,但铁离子水解
Fe3++3H2O?Fe(OH)3+3H+.所以溶液中阳离子数目大于0.1NA,故A错误;
B、NO2气体与水反应3NO2+H2O=2HNO3+NO,常温常压下1molNO2气体反应生成23molHNO3,所以生成23NA个NO3-离子,故B错误;
C、CaCO3与Mg3N2的摩尔质量都是100g/mol,0.6gCaCO3与Mg3N2的混合物的物质的量为0.006mol,每摩尔CaCO3与Mg3N2都含有50mol质子,所以含有的质子数为0.006mol×50×NAmol-1=0.3NA,故C正确.
D、MnO2与浓盐酸反应MnO2+4HCl(浓)?△?.?MnCl2+Cl2↑+2H2O,若80mL10mol/L浓盐酸完全反应,生成氯气为0.08L×10mol/L×14=0.2mol,转移电子数为0.2mol×2×NAmol-1=0.4NA,随反应进行,浓盐酸变为稀盐酸,MnO2与稀盐酸不反应,所以转移电子数小于0.4NA,故D错误.
故选:C.
本题解析:
本题难度:一般
2、选择题 NA表示阿伏加德罗常数,下列叙述正确的足
[? ]
A.等物质的量的N2和CO所含分子数均为NA
B.1.7 g H2O2中含有的电子数为0.9NA
C.1 mol Na2O2晶体中含离子总数为4NA
D.标准状况下,2.24 L戊烷所含分子数为0.1NA
参考答案:B
本题解析:
本题难度:简单
3、选择题 NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.16?g氧气和16?g臭氧所含的原子数均为NA
B.常温常压下,11.2L氯气所含的原子数目为NA
C.2.3g钠由原子变成离子,失去的电子数为1.1?NA
D.28g?N2中所含的质子数目为7?NA
参考答案:A、氧气和臭氧都是氧元素组成的单质,质量相同的单质所含氧元素质量相等;16 g氧气和16 g臭氧所含的原子数相等均为NA,故A正确;
B、常温常压下,11.2L氯气物质的量不是0.5mol,故B错误;
C、2.3g钠由原子变成离子,失电 91eXaM.org子数为0.1mol,故C错误;
D、28g N2中物质的量为1mol,氮原子质子数为7,所以分子中所含的质子数目为14 NA,故D错误;
故选A.
本题解析:
本题难度:简单
4、选择题 用NA表示阿伏加德罗常数的值。下列叙述中完全正确的一组是
[? ]
①常温常压下,1 mol甲基(-CH3)所含的电子数为10NA
②由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成0.2gH2,则电路通过电子0.2NA
③在标准状况下,11.2L NO与11.2L O2混合后气体分子数为0.75NA
④常温常压下,16g O3所含的原子数为NA
⑤1 mol C10H22分子中共价键总数为31 NA
⑥1 mol Cl2发生反应时,转移的电子数一定是2 NA
⑦标准状况下,22.4L水中含分子数为NA
A.①②③④⑤
B.②④⑤⑥⑦
C.②④⑤
D.①②⑤
参考答案:C
本题解析:
本题难度:简单
5、选择题 用NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
A.7.8?g?Na2O2与足量潮湿的CO2反应,转移的电子数为0.1?NA
B.标准状况下2.24?L?HCHO中含0.4?NA个原子
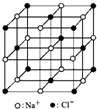
C.23.4?g?NaCl晶体中含0.1?NA个如图所示结构单元
D.CsCl?1mol含晶胞0.25NA个