1、选择题 设NA为阿伏加德罗常数的数值,下列说法正确的是
[? ]
A.常温常压下,16g O3气体含有氧原子数为NA
B.标准状况下,44.8L四氯化碳含有的分子数为2NA
C.0.1mol・L-1氯化铝溶液中含有Al3+数为 0.1 NA
D.2.4g金属镁变为镁离子时失去的电子数为0.1NA
参考答案:A
本题解析:
本题难度:简单
2、选择题 设阿伏加德罗常数的数值为NA,下列说法正确的是( )
A.1molCl2与足量Fe反应,转移的电子数为3NA
B.2mol?Na2O2?与足量H2O反应,转移的电子数为4NA
C.常温常压下,78g的Na2O2?晶体中所含阴离子数为2NA
D.0.10mol?Na与Li的合金跟足量水反应生成H2的分子数为0.05NA
参考答案:A、1molCl2与足量Fe反应,转移的电子数为2NA,故A错误;
B、2mol Na2O2 与足量H2O反应,转移的电子数为2NA,故B错误;
C、78g的Na2O2 晶体物质的量为1mol,含阴离子过氧根离子为1mol,故C错误;
D、钠和锂与水反应都是每2mol金属反应生成1mol氢气,0.10mol Na与Li的合金跟足量水反应生成H2的分子数为0.05NA,故D正确;
故选D.
本题解析:
本题难度:简单
3、选择题 用NA表示阿伏加德罗常数,下列说法正确的是( )
A.48gO2、O3组成的混合物,在任何温度、压强下,不管混合物中各组分的比例,所含的原子数均为3NA
B.在标准状况下,18g水蒸气所占有的体积约为22.4L
C.用浓盐酸与二氧化锰反应制取氯气,若有0.4molHCl被氧化,则可制得氯气4.48L
D.物质的量为1mol的任何物质在任何条件下含有的微观粒子数均为1NA
参考答案:A、48g氧气和臭氧的混合物中含有48g氧原子,含有氧原子的物质的量一定为3mol,所含的原子数均为3NA,故A正确;
B、18g水的物质的量为1mol,标准状况下,水不是气体,题中条件无法计算1mol水的体积,故B错误;
C、用浓盐酸与二氧化锰反应制取氯气,若有0.4molHCl被氧化,反应生成了0.2mol氯气,由于没有告诉是标准状况下,不能使用标况下的气体摩尔体积计算0.2mol氯气的体积,故C错误;
D、必须指出含有的具体粒子名称,否则1mol物质中含有的粒子数不一定为1mol,如1mol氧气中含有2mol氧原子,故D错误;
故选A.
本题解析:
本题难度:简单
4、选择题 用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
A.lmol Na2O2晶体中共含有4NA个离子
B.0.1molAlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒
C.常温常压下16gO2和O3混合气体含有NA个氧原子
D.电解精炼铜时每转移NA个电子,阳极溶解32g铜
参考答案:A、lmolNa2O2晶体中共含有2NANa+和NA022-,故lmolNa2O2晶体中共含有3NA个离子,故A错误;
B、氢氧化铝胶粒是许多氢氧化铝微粒的聚集体,故0.1molAlCl3完全水解转化为氢氧化铝胶体,生成胶粒数小于0.1NA,故B错误;
C、16gO2和O3混合气体含有氧原子的物质的量为:16g16g/mol=1mol,故含NA个氧原子,故C正确;
D、粗铜中比铜活泼的杂质金属如锌铁等也失电子,故电解精炼铜时每转移NA个电子,阳极溶解的铜不是32g,故D错误;
故选:C.
本题解析:
本题难度:一般
5、选择题 设NA?代表阿伏加德?罗常数,下列叙述正确的是
[? ]
A.0.1?mol/L?NaHCO3和0.1?mol/L?Na2CO3混合溶液1L,?HCO3-,CO32-的总数为0.2NA?
B.向密闭容器中充入2molN2和3molH2?,在一定条件下发生反应,达到平衡时,混合气体中NH3的体积分数为23.45%,则H2和NH3所含的H原子总数为6NA?
C.若1L0.1?mol/L的CH3COOH溶液含CH3COO-?数为aNA,?则1L0.3?mol/L的CH3COOH溶液含CH3COO-?数小于0.3aNA
D.反应N2+3H2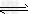 2NH3达平衡时,每形成6NA个N-H键,也生成?14克N2
2NH3达平衡时,每形成6NA个N-H键,也生成?14克N2
参考答案:BD
本题解析:
本题难度:一般