1��ʵ����
ij����С����MnO2��Ũ�����Ʊ�Cl2ʱ�����ø����չ�����SO2��NaOH��Һ����β���������մ�����
(1)�����SO2�����NaOH��Һ��Ӧ�Ļ�ѧ����ʽ��
SO2��2NaOH==?________________________��
(2)��ӦCl2��Na2SO3��2NaOH===2NaCl��Na2SO4��H2O�еĻ�ԭ��Ϊ__________��
(3)����β��һ��ʱ�������Һ(ǿ����)�п϶�����Cl����OH����SO42����
�����ʵ�飬̽��������Һ�п��ܴ��ڵ�����������(�����ǿ�����CO2��Ӱ��)
������������衣
����1��ֻ����SO32����
����2���Ȳ�����SO32����Ҳ������ClO����
����3��____________��
�����ʵ�鷽��������ʵ�顣���ڱ�����д��ʵ�鲽���Լ�Ԥ������ͽ��ۡ���ѡʵ���Լ���3?mol/L?H2SO4��1?mol/L?NaOH��0.01?mol/L?KMnO4�����ۣ�KI��Һ����ɫʯ����Һ��

2��ʵ���� I.ij��ɫ��Һֻ��������8�������е�ij���֣�Na+��H+��Mg2+��Ag+��Cl-��OH-��HCO3-?��NO3-?����֪����Һ����Al2O3��Ӧ����
(1)����Һ��Al2O3��Ӧ����Al3+���ɣ�һ�����Ậ�д�����________?
(2)����Һ��Al2O3��Ӧ����AlO2-?���ɣ����ܺ��д�����____________?
��.�о���ѧϰС���ͬѧΪ���˽�Cu���仯��������ʣ�����������⣻
��Al(OH)3�������ԣ�Cu(OH)2Ҳ����������
��Fe��+2�ۻ�������ȶ��Ա�+3�ۻ�������ȶ���С��Cu��+l�ۻ�������ȶ���Ҳ��+2�ۻ�������ȶ���С��?
(1)����������Ҫ�õ���ҩƷ��CuSO4��Һ��___________?(����ĸ)��
A.AlCl3��Һ?B.NaOH��Һ?C��ϡH2SO4?D��H2O2��Һ
����Cu(OH)2�������ԣ�Ӧ�ÿ�����ʵ��������____________?
(2)Ϊ�˱Ƚ�Cu��+1�ۻ������+2�ۻ�������ȶ��ԣ�����ȡ98gCu(OH)2���壬������800�桫1000��ʱ���õ���ɫ�����ĩ���������ȵ�1?000�����ϣ���ɫ��ĩȫ����ɺ�ɫ��ĩX����ȴ�������X������Ϊ72g����X�м������ϡ���ᣬ�õ���ɫ��Һ��ͬʱ�۲쵽�����л��к�ɫ������ڡ��ݴ˿��Ƶã�X�Ļ�ѧʽΪ__________���Եó��Ľ�����_______________��?
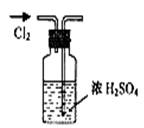
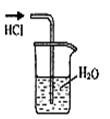
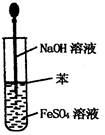
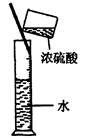
3��ѡ���� ʵ�����о���ѧ�Ļ�������ͼ��ʾ��ʵ�鷽����װ�û������ȫ��ȷ����
 ?
? ?
?
A������Cl2
B������NH3
C����ȡFe(OH)2����
D��ϡ��ŨH2SO4
4��ʵ���� ��ͼװ����ģ�ҵ������ �а��Ĵ��������ش��������⣺
�а��Ĵ��������ش��������⣺
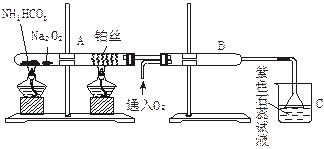
��1�������ȵ��Թ�A��NH4HCO3������Ӧ�Ļ�ѧ����ʽΪ��____________________��
��2�������ȵIJ�˿�������Ļ�ѧ����ʽΪ_______________;��˿��������_______��
��3��B�г��ֵ�����Ϊ��___________________________________________________��
��4���ձ�C�з���������Ϊ________________________________________________��
5��ʵ���� ��1��С���������о��¶ȶԷ�Ӧ���ʵ�Ӱ�족ʵ��ʱ����ȡ����ֻ�Թܣ�������4mL 0��01mol/L��KMnO4������Һ��2mL 0��1mol/L? H2C2O4���Ҷ��ᣩ��Һ����A�Թ�������ˮ�У�B�Թ�������ˮ�У���¼��Һ��ɫ�����ʱ�䡣
����Ҫ����?���ữKMnO4��Һ����ɫ����ʱ��tA?��tB�����������=����������
��д���÷�Ӧ�����ӷ���ʽ��?����
��2��ʵ������ƿ������ɳ���Ҷ�����Ʒ��С�����������Ӧ��ԭ�����ⶨ�京�����������Ϊ��
������250mL��Һ��ȷ����5��0g�Ҷ�����Ʒ�����250mL��Һ��
�ڵζ���ȷ��ȡ25��00mL������Һ����ƿ�У����������ữ����0��1000mol��L��1KMnO4��Һװ��
��?�������ʽ����ʽ�����ζ��ܣ����еζ���������ʵ���з��֣��յ�������KMnO4��Һʱ����ҺѸ�ٱ���Ϻ�ɫ������ƿҡ��һ��ʱ����Ϻ�ɫ������ʧ���ټ����μ�ʱ���Ϻ�ɫ�ͺܿ���ɫ�ˡ������ԭ����?������?��֤���ﵽ�ζ��յ㣮
�ۼ��㣺���ظ���������2�Σ���¼ʵ���������£�
���
| �ζ�ǰ������mL��
| ��������mL��
|
1
| 0��00
| 20��10
|
2
| 1��00
| 20��90
|
3
| 0��00
| 21��10
|
������KMnO4��Һ��ƽ�����Ϊ��?��mL����֪H2C2O4����Է�������Ϊ90�������Ʒ�Ĵ���Ϊ��?����
�������������в����ᵼ�²ⶨ���ƫ�ߵ�����?����
A��δ�ñ�Ũ�ȵ�����KMnO4��Һ��ϴ�ζ���
B���ζ�ǰ��ƿ������ˮ
C���ζ�ǰ�ζ��ܼ��첿�������ݣ��ζ���������ʧ
D����С�Ľ���������KMnO4��Һ������ƿ��
E���۲����ʱ���ζ�ǰ���ӣ��ζ����ӣ�