| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《离子共存》练习题(四)
参考答案:C 本题解析:略 本题难度:一般 2、选择题 浓度为0.50 mol/L的某金属阳离子Mn+的溶液10.00ml ,与0.40 mol/L的NaOH溶液12.50 ml恰好完全反应生成沉淀,则n等于 |
参考答案:A
本题解析:0.50 mol/L的某金属阳离子Mn+的溶液10.00ml的物质的量为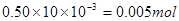 ,0.40 mol/L的NaOH溶液12.50 ml的物质的量为
,0.40 mol/L的NaOH溶液12.50 ml的物质的量为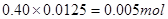 ,所以Mn+的n等于1;
,所以Mn+的n等于1;
本题难度:简单
3、选择题 在某溶液中酚酞呈粉红色。下列离子在该溶液中不能大量存在的是(?)
A.K+
B.Na+
C.Ba2+
D.Al3+
参考答案:D
本题解析:溶液中酚酞呈粉红色,说明该溶液呈碱性,溶液中含有OH-,OH-与Al3+结合生成Al(OH)3沉淀。
本题难度:简单
4、选择题 含下列离子的溶液是无色透明,且离子能大量共存的是
[? ]
参考答案:C
本题解析:
本题难度:一般
5、填空题 (8分)已知某待测液由Ag+、Mg2+、K+、Ba2+、NH4+、NO3-中的若干种离子组成,进行如下实验:第一步:加入过量的稀盐酸,有白色沉淀生成。
第二步:过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
第三步:再过滤,取少量滤液,滴入NaOH溶液至溶液呈碱性,在此过程中溶液无明显现象,加热该溶液,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:
(1)写出第二步中所涉及的反应的离子方程式:
? ;
(2)待测液中一定含有?、NO3-离子,一定不含有?离子,还有一种离子不能确定其是否存在,要检验这种离子的实验方法是(填写实验名称和观察到的现象及结论,不要求写实验操作过程)?,?。
参考答案:(8分)(1) Ba2+ + SO42- = BaSO4↓
(2)一定含有? Ag+ Ba2+ NH4+?、NO3-离子,一定不含有?Mg2+?离子
焰色反应?,透过蓝色钴玻璃片看是否有紫色
本题解析:加入过量的稀盐酸,有白色沉淀生成,则沉淀是氯化银,说明含有银离子;过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成,则沉淀是硫酸钡,说明含有Ba2+;再过滤,取少量滤液,滴入NaOH溶液至溶液呈碱性,在此过程中溶液无明显现象,说明没有镁离子。加热该溶液,可产生使湿润的红色石蕊试纸变蓝色的气体,该气体是氨气,所以含有NH4+。由于溶液是显中性的,所以一定含有NO3-,但钾离子不能确定。而要确定是否含有钾离子,则需要通过焰色反应,需要注意的是要通过蓝色的钴玻璃观察。
点评:进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点大全《分子式、结.. | |