1、选择题 分离下列各组混合物时,可按溶解、过滤、蒸发的操作顺序进行的是
[? ]
A.氯化钠和硝酸钾
B.铁粉和锌粉
C.氯化钾和二氧化锰
D.碳酸铵和氯化铵
2、选择题 下列物质中所含的分子数相等的是
①0.1mol CO2 ?②9.8g H2SO4 ?③1g H2O ?④1.6g O2
A.①②
B.②③
C.①④
D.③④
3、填空题 利用含锰废水(主要含Mn2+、SO42-、H+、Fe2+、Al3+、Cu2+)可制备高性能磁性材料碳酸锰(MnCO3)。其中一种工业流程如下:
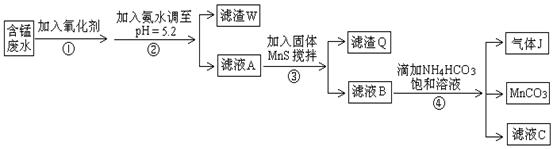
已知某些物质完全沉淀的pH值如下表:
沉淀物
| Fe(OH)3
| Al(OH)3
| Cu(OH)2
| Mn(OH)2
| CuS
| MnS
| MnCO3
|
沉淀完全时的PH
| 3.7
| 5.2
| 6.4
| 9.8
| ≥0
| ≥7
| ≥7
|
回答下列问题:
(1)若下列物质均能把Fe2+氧化为Fe3+,则过程①中可选择加入的氧化剂是?。
a.Cl2?b.MnO2? c.浓HNO3? d.H2O2 ?
(2)过程②中,所得滤渣的成分是?。
(3)过程③中,搅拌的目的是?,发生反应的离子方程式是?。
(4)过程④中,若生成的气体J可使澄清石灰水变浑浊,则生成MnCO3反应的离子方程式是___________。
(5)由MnCO3可制得重要的催化剂MnO2,MnCO3 +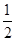 O2 → MnO2 + CO2。
O2 → MnO2 + CO2。
现在空气中加热 460.0 g的MnCO3,得到332.0 g产品,若产品中杂质只有MnO,则该产品中MnO2的质量分数是?。(摩尔质量/g・:MnCO3 115? MnO2 87? MnO 71)
4、选择题 欲使NaCl、NH4Cl和SiO2的混合物分开,其必要的操作为
A.升华、溶解、过滤、蒸发
B.溶解、过滤、蒸发、分液
C.加热、溶解、过滤、结晶
D.溶解、过滤、分馏、结晶
5、选择题 锌和铝都是活泼金属,其氢氧化物均能既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成配合物离子[Zn(NH3)4]2+。除去Al3+中的杂质Zn2+,最好的方法是:(?)
A.加入适量的NaOH溶液,过滤洗涤,再加盐酸
B.加入过量的NaOH溶液,过滤洗涤,再加盐酸
C.加入适量的盐酸溶液,过滤洗涤再加NaOH溶液
D.加入过量的氨水,过滤洗涤,再加盐酸