?
参考答案:①加盐酸、过滤?CaCO3+2HCl=CaCl2+CO2↑+H2O?(1+2分)
②加NaOH溶液,过滤?2Al+2NaOH+2H2O=2NaAlO2+3H2↑?(1+2分)
③加NaHSO3溶液,过滤 ?NaHSO3+HCl=NaCl+H2O+SO2↑ (1+2分)
本题解析:①二氧化硅只和氢氟酸反应,和其他酸不反应;
② 铝既能和酸反应,又能和碱反应;铝和氢氧化钠溶液反应,金属铁不和氢氧化钠;
③ 饱和亚硫酸氢钠,不和二氧化硫反应,却能吸收氯化氢气体。
本题难度:简单
3、实验题 实验是化学的基础。下图为一化学实验装置图,图中,夹持仪器已略去,用“△”表示用酒精灯加热。
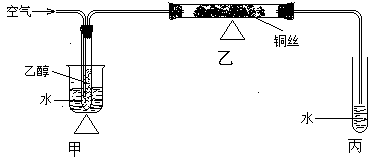
请仔细观察该实验装置图,回答问题:
(1)甲装置通入空气的导气管插入乙醇中的主要目的是?
(2)乙装置用揉乱的铜丝,好处是?
(3)乙装置的化学反应反应方程式为?,反应中,转移电子的数目是?若有23g乙醇发生反应,至少需要通入标准状况下的空气?L
(4)写出一种检验反应产物的方法及现象?
?
(5)该反应还可以用更简便的方法实现:取一束铜丝在酒精灯上加热,铜丝变黑,趁热插入盛有少量乙醇的试管中,铜丝又变红;如此反复多次即可。请写出实验中发生反应的化学方程式?。
参考答案:(1)可以通过观察气泡的流速调节空气的进入量
(2)有利于气体流通,并增加反应接触面积
(3)2CH3CH2OH+O2  2CH3CHO+2H2O? 4e―? 26.7 2CH3CHO+2H2O? 4e―? 26.7
(4)在碱性、加热条件下,与银氨溶液反应析出银(加热条件下,与新制的氢氧化铜反应,产生砖红色沉淀)
(5)2Cu+O2 2CuO? CH3CH2OH+CuO 2CuO? CH3CH2OH+CuO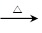 CH3CHO+Cu+H2O CH3CHO+Cu+H2O
本题解析:(1)通入空气的目的是提供氧气氧化乙醇,所以甲装置通入空气的导气管插入乙醇中的主要目的是可以通过观察气泡的流速调节空气的进入量,便于控制反应速率。
(2)乙装置用揉乱的铜丝,好处是有利于气体流通,并增加反应接触面积,加快反应速率。
(3)乙醇发生催化氧化的化学方程式是2CH3CH2OH+O2  2CH3CHO+2H2O,在反应中氧气中氧元素的化合价从0价降低到-2价,所以转移4个电子。23g乙醇的物质的量是23g÷46/mol=0.5mol,消耗氧气是0.5mol÷2=0.25mol,标准状况下的体积是0.25mol×22.4L/mol=5.6L,则需要空气的体积是5.6L÷0.21=26.7L。 2CH3CHO+2H2O,在反应中氧气中氧元素的化合价从0价降低到-2价,所以转移4个电子。23g乙醇的物质的量是23g÷46/mol=0.5mol,消耗氧气是0.5mol÷2=0.25mol,标准状况下的体积是0.25mol×22.4L/mol=5.6L,则需要空气的体积是5.6L÷0.21=26.7L。
(4)乙醇的氧化产物是乙醛,含有醛基,检验醛基的试剂和实验现象是在碱性、加热条件下,与银氨溶液反应析出银(或加热条件下,与新制的氢氧化铜反应,产生砖红色沉淀)。
(5)取一束铜丝在酒精灯上加热,铜丝变黑,这说明铜被氧化生成氧化铜,方程式是2Cu+O2 2CuO。趁热插入盛有少量乙醇的试管中,铜丝又变红,这说明在加热的条件下,氧化铜把乙醇氧化生成乙醛,而氧化铜被还原又生成铜,反应的化学方程式是CH3CH2OH+CuO 2CuO。趁热插入盛有少量乙醇的试管中,铜丝又变红,这说明在加热的条件下,氧化铜把乙醇氧化生成乙醛,而氧化铜被还原又生成铜,反应的化学方程式是CH3CH2OH+CuO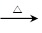 CH3CHO+Cu+H2O。 CH3CHO+Cu+H2O。
点评:该题是高考中的常见题型,属于中等难度的试题,侧重对学生实验能力的培养,有利于培养学生规范严谨的实验设计能力,有助于提升学生的学科素养。该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
本题难度:一般
4、选择题 下列物质分离方法不正确的是( )
A.用四氯化碳萃取碘水中的碘
B.用分液的方法分离酒精和汽油
C.用过滤的方法除去食盐中的泥沙
D.用淘洗的方法从沙里淘金
参考答案:A、四氯化碳不溶于水,碘单质在四氯化碳中的溶解度大于在水中的溶解度,用四氯化碳萃取碘水中的碘,故A正确;
B、汽油和酒精是互溶的,可用蒸馏的方法分离,故B错误;
C、泥沙不溶于水,可用过滤的方法分离,故C正确;
D、从沙里淘金即用水冲洗,滤除杂质,从沙里淘出黄金,属于淘洗法,故D正确.
故选B.
本题解析:
本题难度:一般
5、选择题 用四氯化碳萃取碘水中的碘,下列说法中不正确的是(?)
A.实验使用的主要仪器是分液漏斗
B碘在水中的溶解度比在四氯化碳中小
C碘的四氯化碳溶液呈紫色
D分液时,水从分液漏斗的下口出,碘的四氯化碳溶液从上口倒出
参考答案:D
本题解析:水的密度比四氯化碳小,水在上层,而碘的四氯化碳溶液在下层。所以水应从上口倒出。
本题难度:简单
|