1、选择题 在一定温度下体积固定的密闭容器中,当下列物理量:
①混合气体的压强
②气体的总物质的量
③混合气体的密度
④B的物质的量浓度不再变化时,能表明可逆反应A(s)+2B(g) C(g)+D(g)
C(g)+D(g)
已达平衡的是
[? ]
A.①②
B.①④
C.③④
D.只有④
参考答案:C
本题解析:
本题难度:一般
2、选择题 现向一固定容积密闭容器中充入2mol?N2和3mol?H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g),能说明该反应达到化学平衡状态的是( )
A.N2、H2、NH3的浓度相等
B.容器内N2、H2、NH3混合气体的密度不再变化
C.单位时间内,生成n?mol?N2,同时生成2n?mol?NH3
D.反应停止,正、逆反应速率都等于零
参考答案:A.当N2、H2、NH3的浓度相等时,该反应不一定达到平衡状态,与反应物初始浓度和转化率有关,故A错误;
B.该容器中混合气体的总质量不变,容器的体积不变,所以密度始终不变,则密度不能作为判断平衡状态的依据,故B错误;
C.单位时间内,生成n?mol?N2,同时生成2n?mol?NH3,同时有2nmol氮气参加反应,所以氮气的正逆反应速率相等,该反应达到平衡状态,故C正确;
D.反应达到平衡状态时,正逆反应速率相等但反应不停止且反应速率不为0,故D错误;
故选C.
本题解析:
本题难度:一般
3、选择题 在一定温度下的恒容密闭容器中,当下列量不再发生变化时,不能表明反应A(s)+2B(g) C(g)+D(g)已达化学平衡状态的是(?)?
C(g)+D(g)已达化学平衡状态的是(?)?
A.混合气体的压强
B.混合气体的密度
C.B的物质的量浓度
D.混合气体的摩尔质量
参考答案:A
本题解析:本题考查达到化学平衡状态的标志,综合性较强,考查学生的分析判断能力。
思路如下:A为固态,所以该反应为等体积的反应。在一定温度下的恒容密闭容器中,A项混合气体的压强始终不变,其余三项都变化,只有平衡时,B、C、D三项不变。
本题难度:一般
4、填空题 (14分)下图是煤化工产业链的一部分,试运用所学知识,解决下列问题:
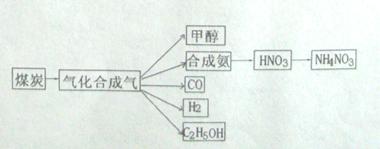
(1)已知该产业链中某反应的平衡表达式为:K=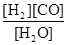 ,它所对应的化学反应为:??
,它所对应的化学反应为:??
(2)已知在一定温度下,各反应的平衡常数如下:
C(s)+C02(g)  2C0(g),K1? ①
2C0(g),K1? ①
CO(g)+H20(g)  H2(g)+C02(g),K2? ?②
H2(g)+C02(g),K2? ?②
C(s)+H20(g)  CO(g)+H2(g),K3? ③
CO(g)+H2(g),K3? ③
则 K1、K2、K3,之间的关系是: ,反应①的平衡常数K随温度的升高而? ?(增大/减小/不变)。
K1、K2、K3,之间的关系是: ,反应①的平衡常数K随温度的升高而? ?(增大/减小/不变)。
一定温度下,在三个容积均为2L的容器中均进行着③反应,各物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。

简述理由:
(3)该产业链中氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如N0、N02、N204等。对反应N2O4(g)  2N02(g) △H>O,在温度为T1、T2时,平衡体系中N02的体积分数随压强变化曲线如图所示。下列说法正确的是(? )
2N02(g) △H>O,在温度为T1、T2时,平衡体系中N02的体积分数随压强变化曲线如图所示。下列说法正确的是(? )

A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
(4)如果(3)中的反应达到平衡后,改变某一外界条件(不改变N204、N02的量),反应速率v与时间t关系如图所示。图中t4时引起平衡移动的条件可能是??;图中表示平衡混合物中N02的含量最高的一段时间是?。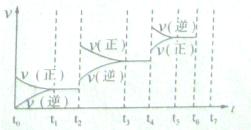
参考答案:

本题解析:略
本题难度:一般
5、填空题 某温度下,在一固定容积的容器中进行如下反应N2+3H2

2NH3,下列情况一定能说明反应已达到限度的是:______.(填序号)
①容器内气压不随时间变化?②1个N≡N键断裂的同时,有6个N-H键断裂③用N2、H2、NH3的物质的量浓度变化表示化学反应速率的比为1:3:2.④容器内气体密度不再改变?⑤混合气的平均相对分子质量不随时间变化.
参考答案:①反应N2+3H2

2NH3是反应前后气体的总物质的量不相等的反应,当体积固定时,根据阿伏伽德罗定律可知,温度、体积相同时,气体的物质的量之比等于压强之比,容器内气压不随时间变化,说明气体的总物质的量不再发生变化,即说明可逆反应达到了化学平衡状态,因此①正确.
②断裂N≡N键代表正反应速率,断裂N-H键代表逆反应速率,其个数比为1:6,即说明用N2代表的正反应速率与用NH3代表的逆反应速率之比为1:2(每个NH3中含有3个N-H键)等于N2与NH3的化学计量数之比,说明正反应速率等于逆反应速率,即②正确.
③不论该可逆反应是否达到化学平衡状态,用N2、H2、NH3的物质的量浓度变化表示化学反应速率的比一定为1:3:2,无法判断是否达到化学平衡状态,即③不正确.
④无论是否达到平衡状态,由于体积不变,气体的总质量不变,其密度都不会发生变化,用密度不变无法区分非平衡状态和平衡状态,因此④不正确.在此提醒:当能用某个量来判断可逆反应达到了化学平衡状态时,该量应该具备的特点是:先变后不变(区分非平衡状态和平衡状态).
⑤混合气体的平均相对分子质量在数值上等于气体的总质量与总物质的量之比,因为总质量不变,当平均相对分子质量不变时,说明总物质的量不再发生变化,与①相同,即⑤正确.
故答案为:①②⑤.
本题解析:
本题难度:一般