1、实验题 下图为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去,已知乙醇的沸点为78.5℃),请根据要求完成下列问题(仪器装置可任意选用,必要时可重复选择,a、b为旋钮)。
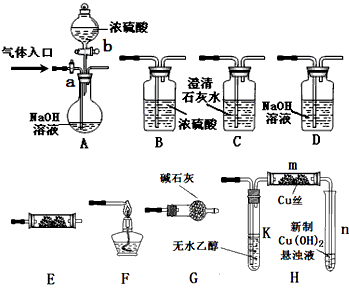
(1)若A中气体入口通入CO和CO2的混合气体,E内放置CuO,欲得到纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为___________ (填写装置代号)。能验证CO氧化产物的实验现象是
________________。
(2)完成(1)实验后,将A中a旋钮关闭,并在E内放置Na2O2,按A→E→D→B→H装置顺序,制取纯净干燥的O2,并用O2氧化乙醇。
①为获得氧气,关闭a旋钮后,首先需进行的操作是_______________。
②为得到平稳的乙醇蒸气流,提高反应效率,可采取的措施是(用文字简述) __________;m中发生反应的化学方程式是____________________________。
③若想观察到试管n中有红色沉淀出现,还需要进行的操作是__________。
参考答案:(1)ACBECF;AB之间的C装置中溶液保持澄清,EF之间的C装置中溶液变浑浊
(2)①打开旋钮b;②将试管K放入水温78.5℃或略高于78.5℃的水浴中加热;2CH3CH2OH+O2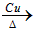
2CH3CHO+2H2O;③取出试管n并用酒精灯加热
本题解析:
本题难度:一般
2、实验题 塑化剂DBP(邻苯二甲酸二丁酯)主要应用于PVC等合成材料中作软化剂。反应原理为:
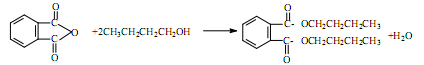
实验步骤如下:
步骤1:在三颈瓶中放入14.8g邻苯二甲酸酐、25mL正丁醇、4滴浓硫酸,开动搅拌器b(反应装置如图)。
步骤2:缓缓加热至邻苯二甲酸酐固体消失,升温至沸腾。
步骤3:等酯化到一定程度时,升温至150℃
步骤4:冷却,将三颈瓶中的液体倒入分漏斗中,用饱和食盐水和5%碳酸钠洗涤。
步骤5:减压蒸馏,收集200~210℃2666Pa馏分,即得DBP产品
(1)浓硫酸的作用?,搅拌器的作用?。
(2)反应过程中正丁醇过量的目的是?。
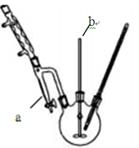
(3)图中仪器a的名称是分水器,试分析它的作用是?。
步骤3中确定有大量酯生成的依据是?。
(4)碳酸钠溶液洗涤的目的是?。
用减压蒸馏的目的是?。
(5)写出正丁醇在135℃生成醚的反应方程式?。
写出DBP在氢氧化钠溶液中水解的方程式?。
参考答案:(共12分)
(1)催化剂、脱水剂,2分,各1分?使反应物充分混合1分
(2)增大正丁醇的含量,可促使反应正向移动,增大邻苯二甲酸酐的转化率1分
(3)及时分离出酯化反应生成的水,促使反应正向移动;1分
分水其中有大量的水生成1分
(4)用碳酸钠除去酯中的醇和酸;1分
减压蒸馏可降低有机物的沸点,可以防止有机物脱水碳化,提高产物的纯度。1分
(5)2CH3(CH2)2CH2OH?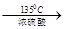 ?= CH3(CH2)3O(CH2)3CH3+H2O
?= CH3(CH2)3O(CH2)3CH3+H2O
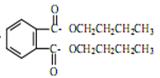 +2NaOH
+2NaOH  2CH3(CH2)2CH2OH+2H2O+
2CH3(CH2)2CH2OH+2H2O+
方程式各2分,条件不写或错误扣1分
本题解析:(1)根据题中信息得,浓硫酸的作用为催化剂、脱水剂。搅拌器的作用为使反应物充分混合。
(2)反应过程中正丁醇过量的目的是增大正丁醇的含量,可促使反应正向移动,增大邻苯二甲酸酐的转化率。
(3)分水器的作用是时分离出酯化反应生成的水,促使反应正向移动。确定有大量酯生成的依据是分水其中有大量的水生成。
(4)碳酸钠溶液洗涤的目的是用碳酸钠除去酯中的醇和酸。用减压蒸馏的目的是减压蒸馏可降低有机物的沸点,可以防止有机物脱水碳化,提高产物的纯度。
(5)根据题中信息得,正丁醇在135℃生成醚的反应方程式为2CH3(CH2)2CH2OH?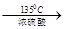 ?= CH3(CH2)3O(CH2)3CH3+H2O。DBP在氢氧化钠溶液中水解的方程式为
?= CH3(CH2)3O(CH2)3CH3+H2O。DBP在氢氧化钠溶液中水解的方程式为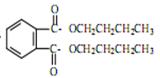 +2NaOH
+2NaOH  2CH3(CH2)2CH2OH+2H2O+
2CH3(CH2)2CH2OH+2H2O+ 。
。
点评:本题考查的是塑化剂的应用和有机反应的相关知识,题目难度大,利用好题中的信息是解题的关键。
本题难度:一般
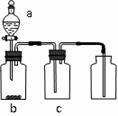
3、选择题 用下图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是
?
| 气体
| a
| b
| c
| 
|
A
| NH3
| 浓氨水
| 氧化钙
| 浓硫酸
|
B
| SO2
| 浓硫酸
| Cu
| 酸性高锰酸钾溶液
|
C
| O2
| 双氧水
| 二氧化锰
| 碱石灰
|
D
| CO2
| 稀盐酸
| CaCO3
| 饱和NaHCO3溶液
|
?
参考答案:D
本题解析:A、氨气的密度小于空气的密度,所以应用向下排空气集气法收集,且不能用浓硫酸干燥氨气,故A不正确;B、浓硫酸和铜反应需要加热才能产生二氧化硫,且酸性高锰酸钾溶液能氧化SO2,故B错误;C、洗气瓶中应该盛放液体干燥剂浓硫酸,C不正确;D、反应装置为固液混合不加热型装置,实验室用碳酸钙和稀盐酸反应制取二氧化碳,且可以用饱和碳酸氢钠溶液除去氯化氢,故D正确,答案选D。
本题难度:一般
4、填空题 (6分)某化工厂排放的污水中含有Mg2+、Fe3+、Cu2+四种离子,甲、乙、丙三位同学设计从污水中回收铜的方案如下:

(1)以上实验方案能否得到铜(填“能”或“不能”):甲_______,乙________。
(2)在可制得铜的方案中,写出所有反应的离子方程式_______________________。
参考答案:(6分)(1)不能 ?能?(各1分,共2分)
(2)Fe+2Fe3+=3Fe2+? Fe+Cu2+=Fe2++Cu?Fe+2H+=Fe2++H2↑?(一个2分,对2个给4分,共4分)
本题解析:略
本题难度:一般
5、实验题 实验室用下图装置制取少量溴苯,试填写下列空白。

(1)在烧瓶a中装的试剂是?、?、?。
(2)请你推测长直导管b的作用是? ??。
(3)请你推测导管c的下口可否浸没于液面中?
(4)写出烧瓶a中所有反应的方程式(标明条件)并指出有机反应类型________。
参考答案:

本题解析:略
本题难度:一般