1、选择题 下列各组离子中,一定能在指定溶液中大量共存的是( )
A.澄清透明的无色溶液:ClO-、CrO42-、Al3+、SO42-
B.能使pH试纸变深蓝色的溶液:Na+、AlO2-、S2-、CO32-
C.常温呈中性的溶液中:Fe3+、K+、Cl-、SO42-
D.能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32-
参考答案:A.CrO42-有颜色,且ClO-与Al3+发生互促水解反应,不能大量共存,故A错误;
B.能使pH试纸变深蓝色的溶液呈碱性,离子之间不发生任何反应,可大量共存,故B正确;
C.Fe3+水解呈酸性,不可能存在于中性溶液中,故C错误;
D.能使淀粉碘化钾试纸显蓝色的溶液具有氧化性,具有还原性的S2-、SO32-不能大量共存,故D错误.
故选B.
本题解析:
本题难度:简单
2、实验题 (18分)以铝灰(主要成分为Al、Al2O3,另有少量CuO、SiO2、FeO和Fe2O3杂质)为原料,可制得液体聚合氯化铝 [Alm(OH)nCl3m―n],生产的部分过程如下图所示(部分产物和操作已略去)。
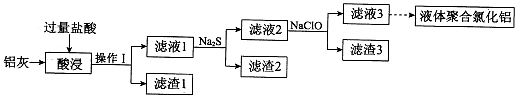
(1)Al2O3与盐酸反应的离子方程式是_____________________。
(2)滤渣I是__________。滤渣2为黑色,该黑色物质的化学式是___________。
(3)向滤液2中加入NaClO溶液至不再产生红褐色沉淀,此时溶液的pH约为3.7。其中NaClO的作用是___________。该过程发生反应的离子方程式为______________。
(4)将滤液3的pH调至4.2~4.5,利用水解反应得到液体聚合氯化铝。该反应的化学方程式为_____________________。
(5)Na2S溶液呈碱性的原因是________(用离子方程式表示)。该溶液中c(Na+)=________。
参考答案:(1)Al2O3+6H+ =2 Al3++3H2O
(2)SiO2 CuS
(3)将Fe2+氧化为Fe3+,使Fe3+转化为Fe(OH)3
2Fe2++ClO―+2H+=2Fe3++Cl―+H2O、Fe3++3ClO―+3H2O=Fe(OH)3↓+3HClO(3分)
(4)mAlCl3+nH2O = Alm(OH)nCl3m-n+nHCl (写“ ”也正确)
”也正确)
(5)S2―+H2O HS―+OH―
HS―+OH―
2c(S2―) + 2c(HS―) + 2c(H2S)或2c(S2―) + c(HS―) + c(OH―) - c(H+) (3分)
本题解析:分析题给信息和流程知,铝灰加过量盐酸酸浸发生的反应为2Al+6H+ =2Al3++3H2、Al2O3+6H+ =2Al3++3H2O、CuO+2H+==Cu2+ +H2O、FeO+2H+==Fe2+ +H2O、Fe 2O3 + 6H+="=2" Fe 3+ + 3H2O,经操作Ⅰ过滤得滤渣1为SiO2,滤液1为氯化铝、氯化铁、氯化铜、氯化亚铁和盐酸的混合液,向其中加入硫化钠生成黑色氯化铜沉淀,过滤得滤渣2为硫化铜,滤液2为氯化铝、氯化铁和氯化亚铁的混合液,向其中加入次氯酸钠,将Fe2+氧化为Fe3+,使Fe3+转化为Fe(OH)3,滤液3可制得液体聚合氯化铝[Alm(OH)nCl3m―n]。(1)Al2O3与盐酸反应生成氯化铝和水,离子方程式是Al2O3+6H+ =2 Al3++3H2O ;(2)滤渣I是SiO2,滤渣2为黑色,该黑色物质的化学式是CuS;(3)向滤液2中加入NaClO溶液至不再产生红褐色沉淀,此时溶液的pH约为3.7。 其中NaClO的作用是将Fe2+氧化为Fe3+,使Fe3+转化为Fe(OH)3 。该过程发生反应的离子方程式为2Fe2++ClO―+2H+=2Fe3++Cl―+H2O、Fe3++3ClO―+3H2O=Fe(OH)3↓+3HClO;(4)将滤液3的pH调至4.2~4.5,利用水解反应得到液体聚合氯化铝。该反应的化学方程式为mAlCl3+nH2O = Alm(OH)nCl3m-n+nHCl;(5)硫化钠为强碱弱酸盐,硫离子分步水解,以第一步水解为主,Na2S溶液呈碱性的原因是S2―+H2O HS―+OH―。该溶液中根据物料守恒有c(Na+)=2c(S2―)+2c(HS―)+2c(H2S),根据电荷守恒有2c(S2―)+c(HS―)+c(OH―)-c(H+)。
HS―+OH―。该溶液中根据物料守恒有c(Na+)=2c(S2―)+2c(HS―)+2c(H2S),根据电荷守恒有2c(S2―)+c(HS―)+c(OH―)-c(H+)。
考点:以液体聚合氯化铝的化工生产流程为载体考查物质的分离、提纯,化学方程式、离子方程式的书写及盐类水解原理的应用。
本题难度:困难
3、选择题 下列各组中的离子,能在溶液中大量共存的是( )
A.K+、Mg2+、NO3-、Cl-
B.Ba2+、Na+、CO32-、OH-
C.Mg2+、Ba2+、OH-、NO3-
D.H+、K+、CO32-、SO42-
参考答案:A、因该组离子之间不反应,则能够大量共存,故A正确;
B、因Ba2+、CO32-能结合生成碳酸钡沉淀,则不能大量共存,故B错误;
C、因Mg2+、OH-能结合生成氢氧化镁沉淀,则不能大量共存,故C错误;
D、因H+、CO32-能结合生成水和二氧化碳气体,则不能大量共存,故D错误;
故选A.
本题解析:
本题难度:一般
4、选择题 某无色溶液中,若加入溴水,溴水褪色,若加入金属铝,铝溶解并产生大量氢气,则该溶液中可能大量存在的离子组是
?
A.Na+、OH―、S 2―、ClO―
B.H+、Na+、Fe2+、NO3―
C.K+、Ba2+、OH―、SO32―
D.Na+、K+、Ba2+、OH-
参考答案:D
本题解析:略
本题难度:简单
5、选择题 下列溶液中因发生氧化还原反应而不能大量共存的是(?)
A.K+ , Cu2+ , Cl- , SO4 2-
B.Fe3+ , Mg2+ , SCN- , SO42-
C.Fe3+ , I- , Ca2+ , Cl-
D.K+ , Ca2+ , CO32- , Cl-
参考答案:C
本题解析:因为Fe3++I-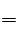 Fe2++I2,Fe3++Cl-
Fe2++I2,Fe3++Cl-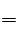 Fe2++Cl2发生了氧化还原反应,满足题意,C正确。
Fe2++Cl2发生了氧化还原反应,满足题意,C正确。
B不能共存是因为Fe3+能与SCN-发生反应,生成沉淀,D不能共存是因为Ca2+和 CO32-生成碳酸钙沉淀,不属于氧化还原反应。
点评:此题通过对离子共存的问题进行考核,重点要求掌握涉及到的反应类型。
本题难度:一般