1��ѡ���� �������ƣ�NaClO2����һ������������Ư��������������Һ�����ֽ⣺ 5HClO2 = 4ClO2�� + H+ + Cl-+ 2H2O��������������Һ�м������ᣬ��Ӧ���ҡ����������Ϊ���ᣬ��ʼʱ��Ӧ����,һ��ʱ����������ٶȽϿ죬�ٶȱ仯��ԭ����
[? ]
A���ݳ�ClO2ʹ������Ũ�Ƚ���
B����ʹ���������������ǿ
C����Һ�е�H+�������
D����Һ�е�Cl-�������
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2��ʵ���� I��������֧�Թ��У���������ֽ�Ļ�ѧ��Ӧ����������?
�Թ�
| �¶�
| ��������Ũ��
| ����
|
a
| ���£�25�棩
| 12%
| ��
|
b
| ˮԡ���ȣ�50�棩
| 4%
| ��
|
c
| ˮԡ���ȣ�50�棩
| 12%
| ��
|
d
| ���£�25�棩
| 4%
| ��
|
II��ijʵ��С����H2O2�ֽ�Ϊ�����о�Ũ�ȡ���������Һ����ԶԷ�Ӧ���ʵ�Ӱ�졣�ڳ����°������·������ʵ�顣
ʵ����
| ��Ӧ��
| ����
|
��
| 10mL2% H2O2��Һ
| ��
|
��
| 10mL5% H2O2��Һ
| ��
|
��
| 10mL5% H2O2��Һ
| 1mL0��1mol��L��1FeCl3��Һ
|
��
| 10mL5% H2O2��Һ������HCl��Һ
| 1mL0��1mol��L��1FeCl3��Һ
|
��
| 10mL5% H2O2��Һ������NaOH��Һ
| 1mL0��1mol��L��1FeCl3��Һ
|
��1��ʵ��ٺ͢ڵ�Ŀ����____________________________��
��2��д��ʵ��۵Ļ�ѧ��Ӧ����ʽ?��
��3��ʵ��ۡ��ܡ����У�������������������ʱ��仯�Ĺ�ϵ��ͼ��
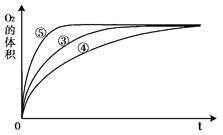
������ͼ�ܹ��ó���ʵ�������?_________________________��
�ο��𰸣�I��c��2�֣�
II����1��̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ��?��2�֣�
��2��2H2O2 O2����2H2O��2�֣�
O2����2H2O��2�֣�
��3�����Ի���������H2O2�ֽ�����ʣ����Ի����ܼ�СH2O2�ֽ������ ��2�֣�
���������I�¶�Խ��ѧ��Ӧ����Խ�����������ѧ��Ӧ�ķ�Ӧ���ʣ����Թ�������ֽ�Ļ�ѧ��Ӧ����������c��
II����1���ٺ͢������ԵĹ��������Ũ�Ȳ�ͬ������������ͬ�����Ԣٺ͢ڵ�Ŀ����̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죻��2��ʵ��۲�����FeCl3��Ϊ����������ʵ��۵Ļ�ѧ��Ӧ����ʽΪ2H2O2 O2����2H2O����ͼ����֪����������NaOH��Һ����Ӧ�ܿ����������������HCl��Һ��Ӧ�������������Է�����ͼ�ܹ��ó��Ľ���Ϊ���Ի���������H2O2�ֽ�����ʣ����Ի����ܼ�СH2O2�ֽ������ ��
O2����2H2O����ͼ����֪����������NaOH��Һ����Ӧ�ܿ����������������HCl��Һ��Ӧ�������������Է�����ͼ�ܹ��ó��Ľ���Ϊ���Ի���������H2O2�ֽ�����ʣ����Ի����ܼ�СH2O2�ֽ������ ��
����������ͨ��ʵ��ķ�ʽ̽����Ӱ�컯ѧ��Ӧ���ʵ����أ����ۺ��ԽϺã�����������ѧ����̽����˼ά�������ѶȲ���
�����Ѷȣ�һ��
3��ѡ���� ������Fe����һ���������ᷴӦ��Ϊ�˼�����Ӧ���ʣ����ֲ�Ӱ�����������������Ӧ�������������еģ�������
A��NaNO3��Һ
B��NaCl����
C��ˮ
D��CuSO4
�ο��𰸣����ݷ����ķ�ӦΪFe+2H+�TFe2++H2�������С�����ӵ�Ũ�ȶ����ı������ӵ����ʵ����������������Ӧ���ʣ����ֲ�Ӱ�����������������
A������NaNO3��Һ��Fe����������ӡ������ӷ���������ԭ��Ӧ����NO������������������A����
B������NaCl���壬�Է�Ӧ��Ӱ�죬���������Ӧ���ʣ���B����
C������ˮ�������ӵ�Ũ�ȼ�С���������ӵ����ʵ���û�б仯����Ӧ���ʼ��������ֲ�Ӱ�������������������C��ȷ��
D������CuSO4������Fe��Cu������ԭ��أ��ӿ췴Ӧ���ʣ���D����
��ѡC��
���������
�����Ѷȣ�һ��
4��ѡ���� ����Zn����50ml�� 0��1mol/L��ϡ�����ַ�Ӧ��Ϊ�˼����˷�Ӧ���ʶ����ı�H2�IJ���������ʹ�����·����еģ� ��
�ټ�Na2SO4��Һ���ڸ���50ml��0��1mol/L��ϡ����۸���50ml��0��05mol/L�����
�ܼ�������������ƣ��ݼ�ѹ���ޱ�ˮԡ����NaCO3��Һ���ിZn��Ϊ������Zn
A���٢ܢ�
B���ۢݢޢߢ�
C���٢ڢݢ�
D��ȫ��