1��ѡ���� ����A��E�������±���������ɵģ������¸����ʴ�1mLϡ�͵�1000mL��pH�ı仯��ϵ����ͼ��ʾ������A��D��Ӧ�õ�E��


����˵������ȷ���ǣ�?��
A������E��NaCl
B������A��NH3��H2O
C������B��NaOH
D������D��CH3COOH
�ο��𰸣�A
�����������
�����Ѷȣ���
2������� ��12�֣���������A��I����ת����ϵ����ͼ����֪��AΪ����Ԫ����ɵĻ����B������ˮ��X������Ϊ��ɫҺ�壬E������Ϊ����ɫ���塣�����ַ�Ӧ���������ɵ�������������ȥ��
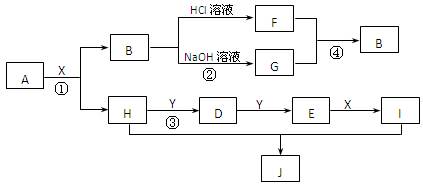
��������ת����ϵͼ�ش�
��1��д���������ʵĻ�ѧʽ X?��J?
��2������H�ĵ���ʽ��?��
����J�������־������ͣ�? ?��
?��
��3��д����Ӧ�ٵĻ�ѧ����ʽ?��
д����Ӧ�ܵ����ӷ���ʽ?��
�ο��𰸣���12�֣�
��1��H2O��? NH4NO3?��2��NH3����ʽ?��?���Ӿ���
��3��AlN+3H2O=Al(OH)3+NH3?�� Al3++3AlO2 -+6H2O="4" Al(OH)3
-+6H2O="4" Al(OH)3
�����������
�����Ѷȣ�һ��
3���ƶ��� A��B��C��D��EΪ��ѧ��ѧ�����ĵ��ʻ���ת����ϵ��ͼ��ʾ �����ֲ�����ȥ����
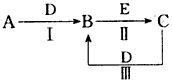
(1)��A����ʹʪ���ɫʯ����ֽ���������壻C��D��Ϊ��������Ҫ�ɷ֣�E��һ���ж����塣
��C�ĵ���ʽΪ________________��
��д����ӦI�Ļ�ѧ����ʽ��________________________��
��д����Ӧ��Ļ�ѧ����ʽ��____________________��
(2)��A�ǵ���ɫ�����������D����ɫ���壻C�к��е����������Ӿ�Ϊ10 �������ӡ�
��D�ĽṹʽΪ___________��C��������ѧ����������_____________��
��д����ӦI�Ļ�ѧ����ʽ��____________________��
��д����Ӧ��Ļ�ѧ����ʽ��____________________��
(3)��(2)��һ����������Dͨ��2 LC����Һ�У���������Һ����μ���ϡ������������������Һ���ȣ�������������HCl���ʵ����Ĺ�ϵ��ͼ��ʾ������������ܽ��HCl�Ļӷ�����
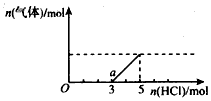
��O����Һ���������ʵĻ�ѧʽΪ________________��������a����Һ��pH____7 ���>����=����<������a����Һ�и�����Ũ���ɴ�С�Ĺ�ϵ��_______________��
�ڱ�״���£�ͨ������D�Ļ���Ϊ_______L��C��Һ�����ʵ���Ũ��Ϊ_________mol/L��
�ο��𰸣�(1)�� ����4NH3+5O2
����4NH3+5O2 4NO+6H2O����2NO+2CO
4NO+6H2O����2NO+2CO N2+2CO2
N2+2CO2
(2)��O=C=O�������ԣ����ۼ������Ӽ�����2Na2O2+2CO2==2Na2CO3+O2����Ca(OH)2+Na2CO3=CaCO3��+2NaOH [��Ba(OH)2����Ca(OH)2��]
(3)��NaOH��Na2CO3��>��c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-)����44.8��2.5
���������
�����Ѷȣ�����
4������� (12��)A��B��C��D��E���������������е�����Ԫ�أ����ǵ�ԭ��������������B��C��D��ͬһ���ڣ�A ��E�����ڱ��д���ͬһ���С���֪:
�ٳ�A�⣬��Ԫ��ԭ�ӵ��ڲ�����������ӣ�����B���������4�����ӣ�
��C�Ļ�̬ԭ�ӵ�2p�ܼ���ԭ�ӹ������2��δ�ɶԵ���(������)��
��D��E�������ӻ���������ӵĵ��Ӳ�ṹ��ͬ���ش�:
��1��AΪ?Ԫ�أ�BΪ?Ԫ�أ�CΪ?Ԫ�أ�DΪ?Ԫ�ء�
��2��CԪ�������ڱ�����?����?��Ԫ�أ�ԭ�ӽṹ��ͼΪ?��
��3���õ���ʽ��ʾD��E�γɻ�����Ĺ���_______________________��д��Eԭ�ӻ�̬�����Ų�ʽ? ______________?��
�ο��𰸣���1����?̼?��?��
��2���ڶ�?��A? (��ԭ��ʾ��ͼ��)
��3��(�õ���ʽ��ʾNaF�γɹ����ԡ�
1s22s22p63s23p64s1
˵�����������ո�2�֣������1��
�����������
�����Ѷȣ���
5������� �ס��ҡ����������������ֶ�����Ԫ�أ���ԭ�����������������ǿ���������п�ͼ�������ʣ������ҡ������Ҿ����γ�ԭ�Ӹ�����Ϊ2��1��1��1�Ļ������Ԫ��ԭ�ӵ�����������������Ӳ�����2������ͼ����ҺMΪ����ɫ����һ�������£����и����ʿɷ�����ͼ��ʾ�ı仯���Իش�
��1����Ԫ�ص�ԭ�ӽṹʾ��ͼΪ______
��2��A�ĵ���ʽΪ______
��3����ҵ����F�Ʊ�H��������______
��4����Ӧ�������ӷ���ʽΪ______��
��5����Ӧ���Ļ�ѧ����ʽΪ______��
�ο��𰸣������ҡ������Ҿ����γ�ԭ�Ӹ�����Ϊ2��1��1��1�Ļ����������������H2O��H2O2��Na2O��Na2O2�ȣ����ΪH����ΪO����ΪNa����Ԫ��ԭ�ӵ�����������������Ӳ�����2������ԭ���������ڱ�����ӦΪS����ҺMΪ����ɫ��ӦΪ������ˮ��Һ��˵����ӦΪClԪ�أ�����F��M��Ӧ����������Һ������MΪ������ӦΪSO2��Cl2�ķ�Ӧ������H2SO4��HCl����FΪSO2����O2��Ӧ�����������ᣬ��DΪO2��HΪSO3��EΪH2SO4��LΪHCl��KӦΪH2O������A��ˮ��Ӧ����O2��ӦΪNa2O2����ˮ��Ӧ������NaOH����CΪNaOH��������SO2��Ӧ����Na2SO3������BӦΪNa2SO3��GΪNa2SO4����
��1����ΪClԪ�أ�ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ7��ԭ�ӽṹʾ��ͼΪ
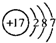
���ʴ�Ϊ��
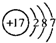
��
��2��AΪNa2O2��Ϊ���ӻ��������ʽΪ
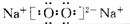
���ʴ�Ϊ��
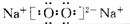
��
��3����ҵ��SO2�Ʊ�SO3���ڳ�ѹ�¡�500���Լ�Ϊ�����������·�Ӧ��
�ʴ�Ϊ����ѹ����������V2O5����500�����ң����£���
��4��CΪNaOH��������SO2��Ӧ����Na2SO3����Ӧ�����ӷ���ʽΪ2OH-+SO2�TSO32-+H2O��
�ʴ�Ϊ��2OH-+SO2�TSO32-+H2O��
��5��SO2��Cl2�ķ�Ӧ������H2SO4��HCl����Ӧ�Ļ�ѧ����ʽΪSO2+Cl2+2H2O=H2SO4+2HCl��
�ʴ�Ϊ��SO2+Cl2+2H2O=H2SO4+2HCl��
���������
�����Ѷȣ���