1、计算题 次磷酸H3PO2是一种强还原剂,将它加入CuSO4水溶液,加热到40~50℃,析出一种红棕色的难溶物A。经鉴定:反应后的溶液是磷酸和硫酸的混合物;X射线衍射证实A是一种六方晶体,结构类同于纤维锌矿(ZnS), 组成稳定;A的主要化学性质如下:1。温度超过60℃,分解成金属铜和一种气体;2。在氯气中着火;3。与盐酸应放出气体。回答如下问题:(1)写出A的化学式。(2)写出A的生成反应方程式。(3)写出A与氯气反应的化学方程式。(4)写出A与盐酸反应的化学方程式。
2、填空题 (12分)氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)下列生产、生活中的事例中发生了氧化还原反应的是
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用如图表达。
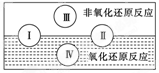
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:?
其中水为________剂。
(3)“细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如溶液中氧化亚铁硫杆菌能利用空气中的氧气将黄铁矿(主要成分FeS2)氧化为Fe2(SO4)3,并使溶液酸性增强。
①该过程反应的化学方程式为__________________________。
②人们可利用Fe2(SO4)3作强氧化剂溶解铜矿石(Cu2S),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:
________Cu2S+________Fe3++______H2O________Cu2++________Fe2++________( )+________SO42-。
(4)羟胺(NH2OH)是一种还原剂,用25.00 mL 0.049 mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与24.5 mL 0.020 mol/L的KMnO4酸性溶液反应。则在上述反应中,羟胺的氧化产物是?。
3、填空题 (5分)将下列性质的序号,填入题后面对应的括号中:
A.脱水性;
B.强酸性;
C.二元酸;
D.强氧化性 E. 吸水性
 的干燥器中,过一段时间胆矾变白色
的干燥器中,过一段时间胆矾变白色 反应,可生成
反应,可生成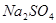 和
和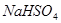 这两种盐
这两种盐 变黑
变黑 中放入铝片就产生NO
中放入铝片就产生NO