1、填空题 (16分) 以电解法生产金属锰产生的阳极泥中,其锰含量高达40%~50%,主要成分为MnO2的水合物,且含有显著量的Pb2+、Sn2+等重金属杂质。本工艺采用的木屑富含的纤维素在较浓硫酸的作用下膨胀、水解生成还原糖,酸性条件下,可与二氧化锰反应生成可溶性的硫酸锰。

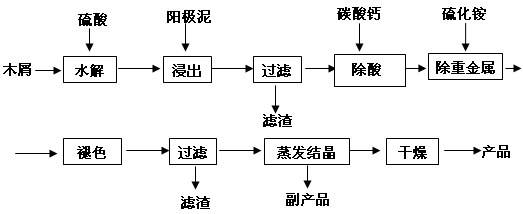
(1)工业上电解硫酸锰的水溶液生产金属锰,阳极的电极反应式为 。
(2)写出木屑水解反应的化学方程式: 。配平浸出步骤反应方程式C6H12O6 + MnO2 + H2SO4→ MnSO4 + CO2 + H2O
(3)若取消除酸操作步骤,将会产生 气体(填化学式)而污染环境;
(4)本工艺的一种副产品是重要的农业生产资料,写出其化学式 ;
(5)取一定量的阳极泥进行实验分析,得到如下图像。硫酸的最合适用量为 mL,若再增加硫酸的用量,将会导致 (填化学式)的消耗量增大。

(6)某阳极泥中MnO2(相对分子质量为87)的质量分数为50.0%,将174g该阳极泥与320g36.5%的浓盐酸混合加热,则产生的氯气在标准状况下应少于 L。(假设阳极泥中的其它成分不参与反应)
参考答案:(1)4OH- -4e-=O2 + 2H2O 或2H2O
本题解析:
本题难度:困难
2、填空题 现有下列十种物质:
①H2;②铝;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁液体;⑧氨水;⑨稀硝酸;⑩Al2(SO4)3
上述各物质按物质的分类方法填写表格的空白处(填物质编号):
分类标准
| 金属单质
| 氧化物
| 溶液
| 胶体
| 电解质
|
属于该类的物质
|
|
|
|
|
|
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-= H2O,该离子反应对应的化学方程式为 。
(3)⑩在水中的电离方程式为 ,
(4)少量的④通入⑥的溶液中反应的离子方程式为 。
(5)②与⑨发生反应的化学方程式为:Al + 4HNO3 = Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是 (填化学式),氧化剂与还原剂的物质的量之比是 ,当有5.4g Al发生反应时,转移电子的物质的量为 。该反应的离子方程式为 。
参考答案:(1)
金属单质
氧化物
溶液
胶体
电解质
属于该类的物质
②
③④
⑧⑨
⑦
③⑤⑥⑩
(2)Ba(OH)2 + 2HNO3 = Ba(NO3)2 + 2H2O
(3)Al2(SO4)3 = 2Al3++ 3SO42-
(4)Ba2++2OH-+CO2 = BaCO3↓+ H2O
(5)HNO3 1
本题解析:
本题难度:一般
3、选择题 下列有关化学用语使用正确的是? (? )
A.NH4Br的电子式: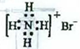
B.S2-的结构示意图:
C.乙酸的分子式:CH3COOH
D.原子核内有18个中子的氯原子:
参考答案:D
本题解析:A选项中溴为阴离子,要打出周围的8个电子,并带一个负电荷。B中原子核标注时需要带正号。C选项为乙酸的结构简式,不是分子式。D正确。
点评:本题为常考题型,比较容易考到的是化学物质的电子式,原子离子的结构示意图,有机物的结构式,结构简式,分子式等。属于简单题
本题难度:一般
4、选择题 含有ag硝酸的稀溶液跟bg铁恰好反应,铁全部溶解,生成NO,已知有a/4克硝酸被还原,则a:b可能是( )
①3:1 ②3:2 ③4:1 ④9:2.
A.①
B.②
C.①③④
D.①④
参考答案:根据公式n=mM,n(Fe)=b56mol,n(HNO3)=a63mol
(1)设生成硝酸亚铁:
3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O
3? ?8
b56mol? ?a63?mol
a:b=3:1
当a:b=3:1时,含有ag硝酸的稀溶液跟bg铁恰好反应,产物为硝酸铁和水.
(2)设生成硝酸铁:
Fe+4HNO3 =Fe(NO3)3+NO↑+2H2O
1? ? 4
b56?mol?a63 mol
a:b=9:2
当a:b=9:2时,含有ag硝酸的稀溶液跟bg铁恰好反应,产物为硝酸亚铁和水.
(3)设硝酸铁、硝酸亚铁和水.此时a:b介于3:1与9:2之间,即3--4.5之间,选项②3:2 不在此范围.
故正确答案为B.
本题解析:
本题难度:一般
5、选择题 芯片是电脑、“智能”加点的核心部件,它是用高纯度硅制成的。下面是生产单质硅过程中的一个重要反应:SiO2 + 2C ="===" Si +2CO↑,该反应的基本类型是
A.化合反应
B.分解反应
C.置换反应
D.复分解反应
参考答案:C
本题解析:
正确答案:C
SiO2 + 2C Si +2CO是化合物+单质=化合物+单质的反应,是置换反应,C正确。
Si +2CO是化合物+单质=化合物+单质的反应,是置换反应,C正确。
本题难度:简单