|
|
|
���л�ѧ֪ʶ���ȫ�����ʵ�������Ƶ������ѵ��2019�����°棩(��)
2019-06-25 23:28:38
�� �� �� ��
|
1��ѡ���� ����˵����ȷ����
A��1mol�κ����ʶ�����Լ6.02��1023������
B�����ʵ����������ʵ������������ʵ�����
C��40gNaOH����1Lˮ�У�������ҺŨ��Ϊ1mol/L
D�������Ħ�������һ����22.4L/mol
|
�ο��𰸣�D
���������A��1mol�κ������ж�����Լ6.02��1023�������������ʵ�����һ���Ƿ��ӣ�����B�����ʵ���ֻ��ʾһ����Ŀ�����ӵļ����壬����ʾ���ʵ����������ʵ�����������C��40gNaOH�����ʵ�����mol��������Lˮ�еõ�����Һ���������L������������ҺŨ�Ȳ�Ϊ1mol/L������D�������Ħ�������һ����22.4L/mol����״���������Ħ�������22.4L/mol�����¶ȡ�ѹǿ�й�ϵ����ȷ����ѡD��
���㣺��������ʵ��������ʵ���Ũ�ȡ�����Ħ��������ж�
�����Ѷȣ�һ��
2������� FeSO4?7H2O�㷺����ҽҩ��ҵ����������FeSO4?7H2O��ʵ�����Ʊ�����ͼ�������������������գ�

��1����������̼������Һ�ܳ�ȥ���ۣ�ԭ����______�������ӷ���ʽ��ʾ����
��2���������ʷ��뷽����ԭ���������ͬ����______���������ĸ����
a������?b����Һ
c������?d���ؽᾧ
��3��FeSO4?7H2O��ijЩ��Ѫ������Ҫ�ɷ֣�ʵ������Ϊ�ⶨij��Ѫ������Ԫ�صĺ���������������ʵ�飺
������100mL 1.00��10-2mol?L-1��KMnO4��Һ�����õ���������ƽ���ձ�����ͷ�ιܼ�______�����ƹ���������˵���У���ȷ����______���������ĸ����
a��KMnO4����ˮ�����ȣ�����ֱ��������ƿ���ܽ�
b������ƿϴ�Ӻ�����T��ֱ������ʵ��
c�����ݺ�ҡ�ȣ���Һ����ڿ̶��ߣ��ټ�ˮ����Һ����͵���̶�����ƽ
d���������ʱ��ˮ�����̶��߱�����������
��ȡ2.0g�˸ò�Ѫ�������Һ������Ԥ������ʹ���е���Ԫ��ȫ����Fe2+���������ƺõı�KMnO4��Һ�����������½���������ԭ�ζ�����Ӧ�����ӷ���ʽ�ǣ�5Fe2++MnO4-+8H+�T5Fe3++Mn2++4H2O�����еζ�ʱ����KMnO4��ҺӦ��ʢ����______�����ʽ����ʽ��֮һ���ζ����У�ԭ����______��
�۵ζ�����ʱ������Ũ��Ϊ1.00��10-2mol?L-1�ı�KMnO4��Һ26.00mL����ò�Ѫ������Ԫ�صĺ���Ϊ______%��
�ο��𰸣���1����������̼������Һ�ܳ�ȥ���ۣ���Һ��̼�������ˮ��Һ��ˮ���Լ��ԣ���Ӧ�����ӷ���ʽΪ��CO32-+H2O?HCO3-+OH-��HCO3-+H2O?H2CO3+OH-��
�ʴ�Ϊ��CO32-+H2O?HCO3-+OH-��HCO3-+H2O?H2CO3+OH-��
��2�����ʷ��뷽����ԭ���������ͬ����������ֽ�ѹ��岻�������Һ���룻�����Է����жϣ�
a�������Ƿ���е㲻ͬ�Ļ�����a�����ϣ�
b����Һ�����û������ܵ�Һ�徲�÷�Һ����b�����ϣ�
c�����������ð�Ĥ������Һ�ͽ��壬����ԭ����ͬ����c���ϣ�?
d���ؽᾧ����������Ũ�����ᾧ��������d�����ϣ�
�ʴ�Ϊ��c��
��3��������100mL 1.00��10-2mol?L-1��KMnO4��Һ�����õ���������ƽ���ձ�����ͷ�ιܡ�100mL����ƿ ��������
a������ƿ���������ܽ����ʣ���a����
b������ƿ��ȷ��������Һ�����ߣ�����ˮ���ݣ�����ƿϴ�Ӻ�����T��ֱ������ʵ�飻��b��ȷ��
c�����ݺ�ҡ�Ⱥ���Ҫ�ټ�ˮ����ˮ����ҺŨ�ȼ�С����c����
d����ˮ�����̶ȣ�����ʧ����Ҫ�������ƣ���d��ȷ��
�ʴ�Ϊ��100mL����ƿ����������bd��
��KMnO4��Һ����ǿ�����ԣ�����ʢ���ڼ�ʽ�ζ��ܣ���Ϊ���������Һ��ʴ�ܣ�����ʢ������ʽ�ζ����У�
�ʴ�Ϊ����ʽ��KMnO4��Һ��ǿ�������ܸ�ʴ�ܣ�
�۵ζ�����ʱ������Ũ��Ϊ1.00��10-2mol?L-1�ı�KMnO4��Һ26.00mL����ʴ�ķ�ӦΪ������Ԫ�����ʵ���Ϊx��
5Fe2++MnO4-+8H+�T5Fe3++Mn2++4H2O��
5? 1
x? 1.00��10-2mol?L-1��0.0260L
x=1.3��10-3mol��
��Ԫ������=1.3��10-3mol��56g/mol=0.0728g
2.0g�˸ò�Ѫ������Ԫ�غ���=0.0728g2.0g��100%=3.64%
�ʴ�Ϊ��3.64��
���������
�����Ѷȣ�һ��
3��ѡ���� ��NA��ʾ����������������������ȷ����(? )
A����״���£�22.4LH2O���еķ�����ΪNA
B��2.7g������������ǿ���ǿ������ʱʧȥ������Ŀ��Ϊ0.3NA
C�����³�ѹ�£�1.06g Na2CO3���庬�е�Na+������Ϊ0.01 NA
D�����ʵ���Ũ��Ϊ0.5 mol/L��MgCl2��Һ�У�����Cl-����ΪNA
�ο��𰸣�B
���������A ����״���£�ˮΪҺ̬
B ��ȷ��2.7g������������ǿ���ǿ�����ã����ϼ۶����ߵ�+3�ۣ����ԣ�ʧȥ������Ŀ��Ϊ0.3NA
C �����³�ѹ�£�1.06g Na2CO3���庬�е�Na+������Ϊ0.02 NA
D ����û�б�����Һ���������������ʵ����ʵ�����
�����Ѷȣ�һ��
4��ѡ���� ������ͬ�����������У��������������ǣ� ��
A��O2
B��NH3
C��CO
D��CH4
|
�ο��𰸣�D
�����������������ʵ�����Ϊ ����
����
A�����������ʵ��� ��
��
B�����������ʵ��� ��
��
C��һ����̼�����ʵ��� ��
��
D����������ʵ��� ��
��
��Ϊ ��
��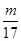 ��
�� ��
�� ���ʺ�������������D��
���ʺ�������������D��
���㣺���ʵ���
���������⿼�������ʵ����ļ��㣬������������㹫ʽ ����ȷ����Ĺؼ������ڻ����⡣
����ȷ����Ĺؼ������ڻ����⡣
�����Ѷȣ���
5��ѡ���� ѧ�������ʵ���Ũ�ȵĸ��������Ϊ1 mol/L������Һ�ĺ���Ӧ��
[? ]
A��ÿ1Lˮ�к���1 mol H2SO4
B��ÿ1L��Һ�к�1 mol H+
C����98 g H2SO4����1Lˮ������ɵ���Һ
D��ָÿ1L������Һ�к���98g H2SO4
�ο��𰸣�D
���������
�����Ѷȣ���
 ����
���� ��
�� ��
�� ��
�� ��
�� ��
��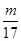 ��
�� ��
�� ���ʺ�������������D��
���ʺ�������������D�� ����ȷ����Ĺؼ������ڻ����⡣
����ȷ����Ĺؼ������ڻ����⡣