1、填空题 某小组用铜屑制取硫酸铜溶液。将铜屑放入一定浓度的硫酸中,加热并不断鼓入空气其反应原理为2Cu+O2+2H2SO4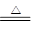 2CuSO4+2H2O。现欲将6.4 g铜完全溶解,加水后得200 mL溶液。计算:
2CuSO4+2H2O。现欲将6.4 g铜完全溶解,加水后得200 mL溶液。计算:
(1)参加反应的氧气在标准状况下的体积是 。
(2)所得硫酸铜溶液的物质的量浓度是 。
(3)取100 mL上述硫酸铜溶液,加水稀释至0.1 mol/L,稀释后硫酸铜溶液的体积是 。
2、选择题 下列溶液中Cl-浓度最大的是( )
A.10ml 0.2mol/L的FeCl3溶液
B.10ml 0.1mol/L的AlCl3溶液
C.20ml 0.1mol/L的MgCl2溶液
D.20ml 0.1mol/L的HCl溶液
3、简答题 用18mol/L浓硫酸配制100ml3.0mol/L稀硫酸的实验有以下步骤:
①计算所用浓硫酸的体积②稀释③量取一定体积的浓硫酸④定容、摇匀⑤转移、洗涤
回答下列问题
(1)上述步骤的正确顺序是______;
(2)本实验用到的玻璃仪器有______;
(3)本实验所需浓硫酸的体积是______ml,
量取浓硫酸所用的量筒的规格是______.(用序号表示)(从下列中选用A.10mlB.25mlC.50mlD.100ml)
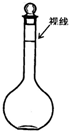
(4)某同学观察液面的情况如图所示,对所配溶液浓度有何影响?(填“偏高”、“偏低”、“无影响”)______;
若没有进行操作步骤⑤,会______(填“偏高”、“偏低”、“无影响”);
(5)若加蒸馏水时不慎超过了刻度线,应如何操作?______.
4、填空题 CO2的摩尔质量是 ;2molCO2的质量是 ;它在标准状况下所占的体积约为 ,所含的分子数目约为 ;所含氧原子的数目约为 。
5、选择题 欲配制100mL1.0mol?L-1Na2SO4溶液,正确的方法是( )
①将14.2gNa2SO4溶于100mL水中
②将32.2gNa2SO4?10H2O溶于少量水中,再用水稀释至100mL
③将20mL5.0mol?L-1Na2SO4溶液用水稀释至100mL.
A.①②
B.②③
C.①③
D.①②③