| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《物质的量》试题预测(2019年最新版)(十)
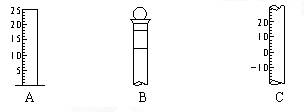 ⑴请写出下列仪器的名称: A ?,B ?,C ??。 ⑵仪器B上标记有?(填序号)。 ①质量?②温度?  ?③刻度线?④浓度?⑤容积 ?③刻度线?④浓度?⑤容积⑶检验仪器B是否漏水的方法是? 参考答案: 本题解析:略 本题难度:一般 2、选择题 在Al2(SO4)3、K2SO4和明矾的混和溶液中,如果c(SO42-)等于0.2mol/L,当加入等体积的0.2mol/L的KOH溶液时,生成的沉淀恰好溶解,则原混和液中K+的物质的浓度为( ) 参考答案:Al2(SO4)3、K2SO4和明矾的混和溶液中,加入等体积的0.2mol/L的KOH溶液时,生成的沉淀恰好溶解,发生反应Al3++4OH-=AlO2-+2H2O,此时溶液中溶质为硫酸钾、偏铝酸钾,根据硫酸根守恒,此时溶液中c(SO42-)=12×0.2mol/L=0.1mol/L,由离子方程式Al3++4OH-=AlO2-+2H2O可知,此时溶液中c(AlO2-)=14×0.2mol/L×12=0.025mol/L,由电荷守恒可知此时溶液中c(K+)=c(AlO2-)+2c(SO42-)=0.025mol/L+2×0.1mol/L=0.225mol/L,所以原混合溶液中为反应后溶液中c(K+)为0.225mol/L×2=0.45mol/L. 本题解析: 本题难度:一般 3、选择题 甲原子与乙原子的质量比为a:b,而乙原子与碳12原子的质量比为c:d,则甲原子的相对原子质量为 参考答案:A 本题解析:元素原子的相对原子质量是该原子质量与碳12原子的质量的1/12的比值。根据题意可知甲原子与碳12原子的质量比为ac:bd,所以甲原子的相对原子质量为12ac/bd,答案选A。 本题难度:一般 4、选择题 现有硫酸钠溶液VmL,它的密度是ρg?mL-1,其中钠离子的质量分数是a%,则有关该溶液的说法不正确的是( )
B.溶液的物质的量浓度是
C.溶质和溶剂的物质的量之比是9a: D.硫酸根离子的质量分数是
参考答案:A.溶液的质量为VmL×ρg?mL-1=Vρg,硫酸钠的物质的量为12×Vρ×a%23mol,质量为12×Vρ×a%23mol×142g/mol,则溶质的质量分数是12×Vρ×a%23×142Vρ×100%=71a23%,故A正确; 本题解析: 本题难度:简单 5、选择题 关于2mol二氧化碳的叙述中,正确的是 ( ) |
参考答案:C
本题解析:A错,质量为88克;B错,标准状况下的体积为44.8L;C正确;D错,含有4mol氧原子;
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《认识晶体》.. | |