1��ѡ���� ��ˮ�Ľ�ˮ��բ���ױ���ʴ���Դ˵�����˵������ȷ����
[? ]
A����բ�Ÿ�ʴ�ı�����Fe-2e-=Fe2+
B����բ�Ÿ�ʴ��Ҫ�Ƿ����绯ѧ������ʴ����������Ӧ��O2+2H2O+4e-=4OH-
C������բ������뺣ˮ��п���õ����������ɷ�ֹ��բ�Ÿ�ʴ
D������բ����ֱ����Դ�������������ɷ�ֹ��բ�Ÿ�ʴ
�ο��𰸣�D
���������
�����Ѷȣ���
2������� X��Y��Z��WΪ��ԭ��������С�������е����ֶ�����Ԫ�ء�
��֪���� X�ɷֱ���Y��W�γ�X2Y��X2Y2��XW�ȹ��ۻ������ Z�ɷֱ���Y��W�γ�Z2Y��Z2Y2��ZW�����ӻ����?
��ش�
��1��Z2Y�Ļ�ѧʽ��?��?
��2��Z2Y2��X2Y��Ӧ�Ļ�ѧ����ʽ��?��
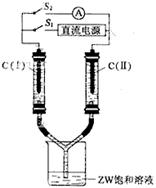
��3����ͼ��ʾװ�ã�����������ʢ�����з�̪��Һ��ZW������Һ��C����C����Ϊ���ʯī�缫��
��ͨS1��C��������Һ��죬�������������������ɡ�?һ��ʱ�������������Һ��δ����缫�����Ͽ�S1����ͨS2����������ָ�뷢��ƫת����ʱ��
C��I���ĵ缫������?����д����������
C��II���ĵ缫��Ӧʽ��??��
��4��ͭм����ϡ���������Ӧ������ϡ�����м���X2Y2��ͭм�����ܽ⣬�÷�Ӧ�����ӷ���ʽ��?��
�ο��𰸣���1��Na2O? (2)2Na2O2+2H2O��4NaOH+O2�� (3)������Cl2+2e-��2Cl-?(4)Cu + H2O2 + 2H+�� Cu2++2H2O
�����������ѧ��A2B2�͵Ļ�������ҪָNa2O2�� H2O2�����ۻ�������H2O2�����ӻ�������Na2O2�����Ը���X��Y��Z��W��ԭ��������С˳����ж�X��H��Y��O��Z��Na��W��Cl��
��1��Z2Y�Ļ�ѧʽ��Na2O��?
��2��Z2Y2��X2Y��Ӧ�Ļ�ѧ����ʽ��2Na2O2+2H2O��4NaOH+O2����
��3������װ��ͼ��֪����ͨS1���װ���ǵ��أ����൱���Ƕ��Ե缫��ⱥ���Ȼ�����Һ��C��������Һ��죬˵���õ缫�����������ɵ�����������������һ�缫���ɵ����������Ͽ�S1����ͨS2����������ָ�뷢��ƫת��˵����ʱ�γ�ԭ��أ������������ڵĵ缫�Ǹ�������C��I���ĵ缫�����Ǹ�����C��II���ĵ缫�������������õ����ӣ��缫��Ӧʽ��Cl2+2e-��2Cl- ��
��4��˫��ˮ���������ԣ�����������ͭ����Ӧ�����ӷ���ʽ��Cu + H2O2 + 2H+�� Cu2++2H2O��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ������Ҫ�ǿ���ѧ���Գ����������Լ��绯ѧԭ������Ϥ�˽�̶ȣ������ڵ���ѧ���������������ͷ�ɢ˼ά���������ѧ��������û���֪ʶ���ʵ�����������������Ĺؼ��Ǽ�ס�����Ļ������ȷԭ��غ͵��صĹ���ԭ����Ȼ��������������ü��ɡ�
�����Ѷȣ�һ��
3������� �������������������ʴ��ÿ����ʴ����ʧ�ĸֲ�ռ�������
�������1/4��
��1��������ʴ��Ҫ��������ʴ���ø�ʴ�����еĵ缫��Ӧʽ��
������?��������?��
��2��Ϊ�˽���ijˮ�����բ�ű���ʴ�����ʣ����Բ�����ͼ��ʾ�ķ��������к�������բ�ŵĹ������R���Բ���?������д������������ƣ�
��3����ͼ���ҷ���Ҳ�ɽ�����բ�Ÿ�ʴ���ʣ�������բ��Ӧ��������ֱ����Դ
��?����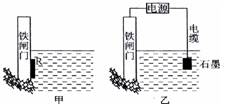
�ο��𰸣���1��������O2+2H2O+4e����4OH����������Fe��2e����Fe2+����2�� п ��3����
�����������
�����Ѷȣ���
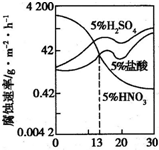
4��ѡ���� ͼ��һϡ���Fe-Gr�Ͻ���Cr�����仯�ĸ�ʴ��ʵ�����������й�˵����ȷ���ǣ�������
A��ϡ�����Fe-Cr�Ͻ�ĸ�ʴ�Ա�ϡ�����ϡ�������
B��ϡ���������Ӧ�Ļ�ѧ����ʽ�ǣ�Fe+6HNO3��ϡ���TFe��NO3��3+3NO2��+3H2O
C��Cr��������13%ʱ����Ϊ�������������������Ũ��������Զ�Fe-Cr�Ͻ�ĸ�ʴ����ǿ
D������Cr�������ӣ�ϡ�����Fe-Cr�Ͻ�ĸ�ʴ�Լ���