1��ѡ���� ���з�Ӧ�У�������������ԭ��Ӧ�����������ӷ�Ӧ���ǣ�������
A����Ƭ��ϡ����ķ�Ӧ
B�������������ķ�Ӧ
C�����ȵ�̿�������̼��Ӧ����һ����̼
D������������Һ��ϡ����ķ�Ӧ
�ο��𰸣�A
�������������:A����Ƭ��ϡ����ķ�Ӧ����������Һ�пɷ��������ӷ�Ӧ����Ӧ�����ӷ���ʽΪ2Al+6H+=3H2��+2Al3+��Ԫ�صĻ��ϼ۷����仯������������ԭ��Ӧ����A���ϣ�
B�������������ķ�Ӧ�������ӷ�Ӧ�����ϼ۷����仯������������ԭ��Ӧ����B�����ϣ�
C�����ȵ�̿�������̼��Ӧ����һ����̼�������ӷ�Ӧ�����ϼ۷����仯������������ԭ��Ӧ����C�����ϣ�
D������������Һ��ϡ����ķ�Ӧ����������Һ�пɷ��������ӷ�Ӧ����Ӧ�����ӷ���ʽΪOH-+H+=H2O����Ԫ�صĻ��ϼ۶�û�з����仯��������������ԭ��Ӧ����D�����ϣ�
���Դ�ѡA
�����Ѷȣ���
2��ѡ���� ��������ǿ�����ԣ���ʹʪ��ĵ⻯�ص�����ֽ�������йط�Ӧ���£�O3+2KI+H2O�T2KOH+I2+O2�����ڴ˷�Ӧ����˵����ȷ���ǣ�������
A����Ӧ��O3����������H2O��KI�ǻ�ԭ��
B���ڷ�Ӧ�У�ÿ����1molO3ת��2mol����
C����������I2�ͻ�ԭ����O2�����ʵ���֮��Ϊ1��1
D���ɴ˷�Ӧ��֪��������ǿ��˳��ΪO3��I2��O2
�ο��𰸣�A��IԪ�صĻ��ϼ����ߣ�OԪ�صĻ��ϼ۽��ͣ���Ӧ��O3����������KI�ǻ�ԭ������A����
B���÷�Ӧ��ת��2e-�����ڷ�Ӧ�У�ÿ����1molO3ת��2mol���ӣ���B��ȷ��
C����������I2�ͻ�ԭ����KOH�����ʵ���֮��Ϊ1��1����C����
D�����������������Դ�����������������Կ�֪��������ǿ��˳��ΪO3��I2������ȷ���������Ĺ�ϵ����D����
��ѡB��
���������
�����Ѷȣ���
3��ѡ���� ���������ڵ�����2%ת��Ϊ�����Լ�ǿ�Ļ���������Щ�������ܼ�������˥�ϣ�����Ϊ������ɱ�֡����й���ѧ�ҳ�����Na2SeO3��������ڵĻ���������Na2SeO3�������ǣ�������
A����ԭ��
B��������
C���������������ǻ�ԭ��
D�����Ͼ�����
�ο��𰸣����������������Լ�ǿ�����ú���Ԫ�أ�Se���Ļ������������ƣ�Na2SeO3��������������ȵĻ�����������Na2SeO3�ܽ�������������ԭ������������Ϊ��������Na2SeO3 Ϊ��ԭ������ѡA��
���������
�����Ѷȣ�һ��
4������� ��֪ͭ�ڳ������ܱ�ϡ�����ܽ⣬��Ӧ����ʽΪ��3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O
��1���õ����ŷ�������ӵ�ʧ�ķ������Ŀ______
��2��������Ӧ����������______������������______��û�вμ�������ԭ��Ӧ������ռ�������______��
�ο��𰸣���1�����ϼ�����Ԫ��Cuʧ���ӣ����ϼ۽���Ԫ��N�õ����ӣ����ϼ�������=���ϼ۽�����=ת�Ƶ�����=6������ת��������£�
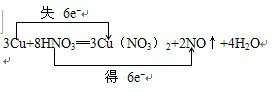
���ʴ�Ϊ��
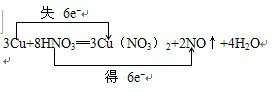
��
��2�����ϼ۽���Ԫ�����ڵķ�Ӧ��HNO3�������������ϼ�����Ԫ��Cu���ڵķ�Ӧ���ǻ�ԭ������Ӧ����Cu��NO3��2�����������8mol�������У�ֻ��2mol��������������6mol����ԭ����û�вμ�������ԭ��Ӧ������ռ�������68����34���ʴ�Ϊ��HNO3��Cu��NO3��2��34��
���������
�����Ѷȣ���
5������� ��1����S+2KNO3+3C=K2S+N2+3CO2�ķ�Ӧ��______Ԫ�ر�������______Ԫ�ر���ԭ��______����������______�ǻ�ԭ����______���������______�ǻ�ԭ���
��2��ij����A��һ�������¼��ȷֽ⣬���ﶼ�����壬�ֽⷽ��ʽΪ��
2A��s��=B��g��+2C��g��+2D��g����ȡһ������A���ȣ���ȫ�ֽ⣬ͬ��ͬѹ�²�����ɵĻ�����������������ܶ�Ϊd����A����Է�������Ϊ______��
��3������A��B��C��D��ƿ��Һ�����Ƿֱ���NaCl��0.1mol?L-1����HCl��0.1mol?L-1����NaOH��0.1mol?L-1���ͷ�̪��Һ��0.1%���е�һ�֣����˲��������Լ����Ϳ�������һһ����������ʵ�鲽�����£�
�ٸ�ȡ��Һ����������ϣ�������ͬ�ֳ����飻
��ȡһ����Һ�����ϵ�����һ���һ��δ֪��Һ����������ͬ�ɼ����A��B������Һ��
����ȡ�Ѽ����A��Һ2mL������3��δ֪C��Һ���ټ���D��Һ4mL���������������������ɫ�仯��
�ۺ�����ʵ���֪��A��B��C��D��Һ�ֱ��ǣ�
A______��?B______��?C______��?D______��
�ο��𰸣��⣨1���ڷ�Ӧ2KNO3+3C+S=K2S+N2��+3CO2���У�NԪ�صĻ��ϼ���+5����Ϊ0��SԪ�صĻ��ϼ���0����Ϊ-2�ۣ���KNO3��S��������������ԭ��Ԫ��ΪN��S��K2S��N2�ǻ�ԭ���CԪ�صĻ��ϼ���0���ߵ�+4����C����ԭ��������������Ӧ��CO2Ϊ��������ʴ�Ϊ��C��S��N��S��KNO3��C��CO2��K2S��N2��
��2����ͬ�����£��������Է���������������ܶȳ����ȣ��������������ƽ����Է�������Ϊ2d���ұ���Է��������ܺ�Ϊ5��d=10d�����������غ㶨�ɣ����2A������Ҳ��10d�����ԣ�A����Է�������Ϊ5d��
�ʴ�Ϊ��5d��
��3��������Ȼ�������̪��ɫ���䣬������������̪��Ϊ��ɫ�����Է�Ϊ�����ǣ�������Ȼ���һ�飬�������ƺͷ�̪һ�飬�������ƺͷ�̪���Ժ�ɫ����Һ�У���������ʱ����ɫ��Ӻ�ɫ��Ϊ��ɫ�����Ȼ���ʱ��Һ����ɫ���䣬���Կ����ȼ����A�����ᣬB���Ȼ��ƣ��������м����̪ʱ����Һ��ɫ���ټ�����������ʱ����Һ�����ɫ��Ϊ��ɫ���������������������ɫ�仯������C���������ƣ�D�Ƿ�̪��
�ʴ�Ϊ��HCl��NaCl��NaOH����̪��
���������
�����Ѷȣ�һ��