1、选择题 室温下,把1 mL 0.1 mol・L-1的H2SO4加水稀释成2 L溶液,在此溶液中由水电离产生的H+,其浓度接近于
A.1×10-4 mol・L-1
B.1×10-8 mol・L-1
C.1×10-11 mol・L-1
D.1×10-10 mol・L-1
2、选择题 常温下,将一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
实验编号
| c(HA)/mol・L-1
| c(NaOH)/mol・L-1
| 混合溶液的pH
|
甲
| 0.1
| 0.1
| pH=a
|
乙
| 0.2
| 0.2
| pH=9
|
丙
| c1
| 0.2
| pH=7
|
丁
| 0.2
| 0.1
| pH<7
|
?
下列判断正确的是
A.a>9
B.在乙组混合液中由水电离出的c(OH-)=10-5mol・L-1
C.c1<0.2
D.丁组混合液:c(Na+)>c(A-)>c(H+)>c(OH-)
3、实验题 某化学实验小组从市场上买来一瓶某品牌食用白醋(主要是醋酸的水溶液),用实验室标准NaOH溶液对其进行滴定以测定它的准确浓度。下表是4种常见指示剂的变色范围:
指示剂
| 石蕊
| 甲基橙
| 甲基红
| 酚酞
|
变色范围(pH)
| 5.0~8.0
| 3.1~4.4
| 4.4~6.2
| 8.2~10.0
|
?
(1)该实验应选用?作指示剂。
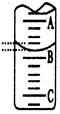
(2)如图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为?mL;反应达滴定终点时的现象为?。
(3)为减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下:
实验次数
| 第一次
| 第二次
| 第三次
|
消耗NaOH溶液体积/mL
| 26.02
| 25.35
| 25.30
|
?
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是?。
A.实验结束时,俯视刻度线读取滴定终点时NaOH溶液的体积;
B.滴定前滴定管尖嘴有气泡,滴定结束尖嘴部分充满溶液;
C.盛装白醋溶液的滴定管用蒸馏水洗过,未用白醋溶液润洗;
D.锥形瓶预先用食用白醋润洗过;
E.滴加NaOH溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定。
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不用化简):C1=?mol/L。
4、选择题 在200 mL某硫酸盐溶液中含有1.5 NA个硫酸根离子(NA表示阿伏加德罗常数),同时含有NA个金属阳离子,则该硫酸盐的物质的量浓度为(? )
A.1 mol・L-1
B.2.5 mol・L-1
C.5 mol・L-1
D.2 mol・L-1
5、选择题 在298K、101kPa时,已知:H2O(g) ===? H2O(l);△H1
C2H5OH(g) ="==" C2H5OH(l);△H2?C2H5OH(g)+3O2(g) ="==" 2CO2(g)+3H2O(g);△H3
则酒精的燃烧热△H =
A.△H1+△H2+2△H3
B.△H1―△H2+△H3
C.3△H1+△H2+△H3
D.3△H1―△H2+△H3