1��ѡ���� ���л�ѧ������ȷ���ǣ�������
A����SiO2����ΪʯӢ�ķ���ʽ
B��1-�����Ľṹ��ʽ��C3H7OH
C����Na-O-O-Na����Ϊ�������ƵĽṹʽ
D��35Br-���ӵĽṹ��ͼ��
�ο��𰸣�D
���������
�����Ѷȣ���
2������� �ش���������
��1��������ԭ�ӵ�ԭ�ӽṹʾ��ͼ��______��
��2��д��H2S���ӵĵ���ʽ��______��
��3��д����ʾ����8�����ӣ�10�����ӵ�ԭ�ӵĻ�ѧ���ţ�______��
��4����֪������aXm-��������bYn+������ͬ�ĺ�������Ų�����a��b��m��n֮��Ĺ�ϵΪa=______��
��5���õ���ʽ��ʾ�Ȼ�þ���γɹ��̣�______��
��6��д��Na2O2��������ѧ��������______��
��7����1mol?H-H����1mol?N-H����1molN��N���ֱ���Ҫ���յ�����Ϊ436kJ��391kJ��946kJ��
��1mol?N2��ȫת����NH3______����������ա��ų�����______kJ��
��8���������з�Ӧ��Fe+Cu2+=Fe?2++Cu?��һ����ѧ��أ�д���缫��Ӧʽ��
������______������______��
�ο��𰸣���1�����ݺ�����Ӳ��Ų�����ԭ�ӵĽṹʾ��ͼΪ��
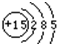
���ʴ�Ϊ
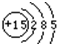
��?
��2��H2SΪ���ۻ��������ʽΪ
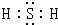
���ʴ�Ϊ��
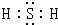
��
��3����ԭ����8�����ӣ���������Ԫ�أ�������Ϊ10�����Ը�ԭ�ӱ�ʾΪ818O���ʴ�Ϊ��818O��?
��4�����������У��˵����=���������+������������������У��˵����=���������-�����������������Xm-��������Yn+�ĺ�������Ų���ͬ������������ͬ������a+m=b-n����a=b-n-m���ʴ�Ϊ��b-n-m��
��5���Ȼ�þ����1��þԭ�Ӻ�2����ԭ��ͨ�����Ӽ��γɵģ��γɹ���Ϊ��

��
�ʴ�Ϊ��

��6������������м��������Ӻ���������֮������Ӽ�������ԭ�Ӻ���ԭ��֮��Ĺ��ۼ����ʴ�Ϊ�����Ӽ����Ǽ��Լ���
��7����Ӧ�ķ���ʽΪ��N2+3H2?2NH3��1molN2��ȫ��Ӧת��ΪNH3��Ӧ��Ϊ��946kJ+3��436kJ-6��391kJ=-92kJ�����Է�Ӧ�ų��������ʴ�Ϊ���ų���92��
��8������ʱ��������ӦʽΪCu2++2e-=Cu��������ӦʽΪZn-2e-=Zn2+���ʴ�Ϊ��Fe-2e-�TFe2+��Cu2++2e-�TCu
���������
�����Ѷȣ�һ��
3������� ��1���������м������ӵĽṹʾ��ͼ���ش����⣺
���������������ӵ���______�����ڽ���Ԫ�ص���______�������ţ�
����д��A��C��D����Ԫ���γɵ�һ�ֻ�������ˮ��Һ�еĵ��뷽��ʽ______��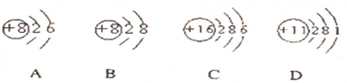
�ο��𰸣������������ӵ���B��ΪO2-�����ڽ���Ԫ�ص���D��ΪNa���ʴ�Ϊ��B��D��
��A��C��D�ĺ����������ֱ�Ϊ8��16��11����������Ԫ��ΪO��S��Na���γɵĻ�����ΪNa2SO4��Na2SO3����ʹ�����Ե����Σ�Ϊǿ����ʣ����뷽��ʽΪ��Na2SO4�T2Na++SO42-����Na2SO3�T2Na++SO32-����
�ʴ�Ϊ��Na2SO4�T2Na++SO42-����Na2SO3�T2Na++SO32-����
���������
�����Ѷȣ�һ��
4������� ���л�ѧ�������д����ȷ���ǣ�������
A����ϩ�Ľṹ��ʽ��CH2CH2
B�������ӵĽṹʾ��ͼ��
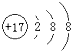
C���廯�Ƶĵ���ʽ��
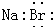
D������ķ���ʽ��C7H16
�ο��𰸣�A����ϩ�Ľṹ��ʽΪCH2=CH2����A����
B�������Ӻ�����3�����Ӳ㣬�������8�����ӣ�������17�����ӣ����������ӽṹʾ��ͼΪ��
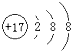
����B��ȷ��
C��NaBr�ĵ���ʽΪ
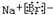
����C����
D������ķ���ʽΪC8H18����D����
��ѡB��
���������
�����Ѷȣ�һ��
5������� �м���Ԫ�ص����ĺ�������Ų���ͼ��ʾ�����У�
��1��ij��������һ�㲻������Ԫ�ص�ԭ�ӷ�Ӧ��������������______��
��2��ij��������Һ������AgNO3��Һʱ����ְ�ɫ���ǣ�������������______��
��3��ij�����������������õ����Ӻ�ԭ��ǿ��������ԭ����һ�������ӣ�������������______��
��4��ij�����л�ԭ�ԣ���������ʧȥ2�����Ӽ���Ϊԭ�ӣ��������ķ�����______��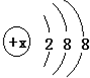
�ο��𰸣���1�����������֪������������ѧ�����ȶ����Ǿ����ȶ��ṹԭ�ӣ����������ں��������Ϊ18��������ΪAr���ʴ�Ϊ��Ar��
��2�����ɫ�������Ȼ��������Ը������������ӣ��ʴ�Ϊ��Cl-��
��3���������������ǵõ��������˵���������ӱȽ��٣�ֻ��1��2��������ʧȥ��һ����+1��+2�ۣ�������ԭ����һ�������ӣ������Ǽ�ԭ�ӣ��ʴ�Ϊ��K��
��4������ij�����л�ԭ�ԣ���ʧȥ2�����Ӻ���ԭ�ӣ�������16��Ԫ�أ��ʴ�Ϊ��S2-��
���������
�����Ѷȣ�һ��