1、简答题 下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族
周期 | IA | | 0
1
①
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2
②
③
④
3
⑤
⑥
⑦
⑧
|
(1)④、⑤、⑥的原子半径由大到小的顺序为______(用元素符号表示).
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的电子式:______.
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)______.
a.MnO2 b.AlCl3 c.Na2SO3? d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
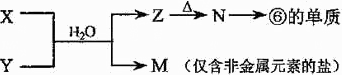
X溶液与Y溶液反应的离子方程式为______,N→⑥的单质的化学方程式为______.
(6)已知破坏1mol?N≡N键、H-H键、N-H键分别需要吸收的能量为946kJ、436kJ、391kJ.则1molN2完全反应转化为NH3共______(填“吸收”或“放出”)能量______?kJ.
2、填空题 在化学符号ZAX中,A表示?_____;Z表示______。
3、选择题 下列物质中属于既能和盐酸又能和氢氧化钠溶液反应的化合物的是(?)
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3 ⑤ NaHSO4 ⑥Mg(OH)2?
A.①②③④⑤
B.②③④
C.③④⑤⑥
D.②③④⑤
4、选择题 下列关于稀有气体的叙述中,不正确的是
[? ]
A.原子的最外电子层都有8个电子
B.其原子与同周期ⅥA、ⅦA族元素形成的阴离子具有相同的核外电子排布
C.通常条件下,化学性质非常不活泼?
D.原子核外电子的排布都达到了稳定结构
5、选择题 下列离子半径比大于1的是
[? ]
A.r(F-)/r(Mg2+)
B.r(Na+)/r(Mg2+)
C.r(Na+)/r(F-)
D.r(Mg2+)/r(Na+)