1、选择题 下列反应中,属于吸热反应的是
A.活泼金属跟酸反应
B.煤气燃烧
C.酸碱中和反应
D.工业制生石灰
参考答案:D
本题解析:A.活泼金属跟酸反应是氧化还原反应,都是放热反应。错误。B.煤气燃烧的反应是放热反应。错误。C.酸碱中和反应是放热反应。错误。D.在工业上一般是用煅烧石灰石来制生石灰。石灰石分解的反应是吸热反应。正确。
本题难度:简单
2、选择题 关于下列各图的叙述,正确的是

A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6 kJ/mol
B.乙表示恒温恒容条件下发生的可逆反应2NO2(g)  N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
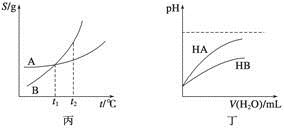
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1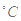 升温至t2
升温至t2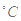 时,溶质的质量分数B>A
时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液
参考答案:D
本题解析:A、H2的燃烧热是指生成液态水时放出的热量,A错误;B、平衡时用NO2和N2O4表示的反应速率应为2:1的关系,B错误;C、由t1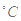 升温至t2
升温至t2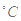 时,溶质的质量分数相等,C错误;D正确,酸或碱稀释相同倍数酸性或碱性强的pH变化范围大。
时,溶质的质量分数相等,C错误;D正确,酸或碱稀释相同倍数酸性或碱性强的pH变化范围大。
本题难度:一般
3、选择题 下列说法不正确的是
A.赤潮、白色污染、绿色食品中的“赤”“白”“绿”均指相关物质的颜色
B.可以用Si3N4、Al2O3制作高温结构陶瓷制品
C.污水处理的方法有多种,常用的化学方法有:混凝法、中和法、沉淀法
D.?是世界通用的循环再生标志,简称回收标志
参考答案:A
本题解析:分析:A.绿色食品是指无化学污染的食品,与颜色无关;
B.Si3N4、Al2O3熔点较高,硬度较大;
C.根据污水中含有的离子以及溶液的酸碱性选择处理方法;
D. 为垃圾回收标志.
为垃圾回收标志.
解答:A.绿色食品是指无化学污染的食品,与颜色无关,白色污染通常实质聚乙烯材料造成的环境污染,但塑料比一定为白色,故A错误;
B.Si3N4为原子晶体,Al2O3为离子晶体,二者的熔点较高,都可制作高温结构陶瓷制品,故B正确;
C.混凝法是利用了胶体的凝聚作用,中和法是利用中和反应调节污水的pH,沉淀法是利用化学反应使重金属离子生成沉淀而除去,都可用于废水处理,故C正确;
D. 为垃圾回收标志,通常是指可循环利用的废弃物,故D正确.
为垃圾回收标志,通常是指可循环利用的废弃物,故D正确.
故选A.
点评:本题考查环境污染及处理方法,注意物质的性质以及对环境的污染,把握常见环境污染种类、原因以及处理方法,题目难度不大.
本题难度:简单
4、选择题 化学反应H2+Cl2===2HCl的能量变化如图所示,则下列说法正确的是

A.该反应是放热反应
B.断裂1 mol H―H键和1 mol Cl―Cl 键放出x kJ能量
C.断裂1 mol H―Cl键需要吸收y kJ的能量
D.2 mol HCl的总能量高于1 mol H2和1 molCl2的总能量
参考答案:A
本题解析:根据图像可知,反应物的总能量高于生成物的总能量,所以反应是放热反应,A正确,D不正确;断键是吸热的,B不正确;根据图像可知,断裂1 mol H―Cl键需要吸收y/2kJ的能量,C不正确,答案选A。
点评:该题是基础性试题的考查,主要是考查学生对反应热含义以及反应热计算的熟悉了解程度,旨在巩固学生的基础,提高学生的应试能力。明确反应热与反应物和生成物总能量的相对大小以及化学键变化时热量的变化是答题的关键,有利于培养学生的逻辑推理能力。
本题难度:一般
5、选择题 下列变化过程中表示的能量转化关系错误的是(?)
A.植物光合作用:光能→生物质能
B.电灯发光:电能→化学能
C.木柴烧饭:生物质能→热能
D.太阳能热水器:光能→热能
参考答案:B
本题解析:电灯发光时,电能主要是转化为光能,部分转化为热能,但不可能转化为化学能,选项B不正确,其余选项都是正确的,答案选B。
点评:该题是常识性知识的检验,难度不大。主要是考查学生对常见能量转化的熟悉了解程度,旨在调动学生的学习兴趣和学习积极性,提高学生的应试能力。
本题难度:简单