1、填空题 (10分) (1)CH4与CO2的混合气体的密度是相同条件下H2密度的14倍,则混合气体的平均摩尔质量为?,CH4与CO2的分子个数比为?。对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的。
(2)现有下列6种物质:CO2、SiO2、CaO、MgO、Fe2O3、C。
按照不同的分类标准,它们中有一种物质与其他5种有明显的不同,请找出这种物质,并写出依据(写出两种分类方法):
①________________________________________②________________________________________。
(3)从上述物质中分别找出两种能相互反应的物质, 各写一个非氧化还原
各写一个非氧化还原 反应的方程式和氧化还原反应的方程式:________________________________,____________________________________
反应的方程式和氧化还原反应的方程式:________________________________,____________________________________
(4)生活中的食醋和淀粉溶液分别属于分散系中的_____和______,用___________可以鉴别(填化学专用名词)。
参考答案:
本题解析:略
本题难度:一般
2、简答题 实验室需用CuSO4?5H2O体配制480mL0.1mol/L的CuSO4溶液,请回答下列问题:
(1)应用托盘天平称取CuSO4?5H2O晶体______g.
(2)若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上(1g以下使用游码),天平平衡时,实际称量的CuSO4?5H2O晶体是______g.
(3)本实验用到的主要仪器有:托盘天平、量筒、烧杯、玻璃棒、______、______.
(4)配制过程中有几个关键的步骤和操作如下图所示:将这些实验步骤A-F按实验过程先后次序排列______.
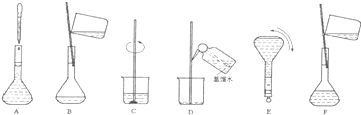
其中定容的具体操作是______.
(5)以下情况会使所配溶液的浓度产生何种影响(A.偏高?B.偏低?C.不变,填序号.):
①溶解晶体用的烧杯和玻璃棒未洗涤.______
②定容时俯视刻度线.______
③所用CuSO4?5H2O晶体已失去部分结晶水.______.
参考答案:(1)配制溶液的体积为480ml,而容量瓶的规格没有480ml,只能选用500ml容量瓶,CuSO4的物质的量n=cV=0.5L×0.1mol?L-1=0.05mol,CuSO4?5H2O的物质的量等于CuSO4的物质的量,所以CuSO4?5H2O的质量0.05mol×250g/mol=12.5g,故答案为:12.5;
(2)若药品与砝码放反,根据天平平衡原理m(左盘)=m(右盘)+游码读数,故实际称量硫酸铜晶体的质量为12g-0.5g=11.5g,故答案为:11.5;
(3)溶液配制一般步骤是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀→装瓶贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,并用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀,
所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,
所以还需要的仪器为:500mL容量瓶、药匙、胶头滴管,
故答案为:500mL容量瓶;药匙、胶头滴管;
(4)由(3)中溶液配制的一般步骤可知,正确的操作顺序为:CBDFAE,
其中定容的具体操作是:向容量瓶中加入蒸馏水,到液面离刻度线1~2cm处时,改用胶头滴管加蒸馏水至凹液面最低点与刻度线相切.
故答案为:CBDFAE;向容量瓶中加入蒸馏水,到液面离刻度线1~2cm处时,改用胶头滴管加蒸馏水至凹液面最低点与刻度线相切;
(5)①溶解晶体用的烧杯和玻璃棒未洗涤,少量硫酸铜沾在烧杯壁与玻璃棒上,移入容量瓶内硫酸铜的物质的量减少,所配溶液的浓度偏低,故答案为:B;
②定容时俯视刻度线,液面在刻度线下方,溶液的体积偏小,所配溶液的浓度偏高,故答案为:A;
③所用CuSO4?5H2O晶体已失去部分结晶水,硫酸铜的质量分数增大,实际称量的硫酸铜晶体中硫酸铜的质量偏大,所配溶液的浓度偏高,故答案为:A.
本题解析:
本题难度:一般
3、选择题 用NA代表阿伏加德罗常数,下列说法正确的是(?)
A.常温下,2LpH=12的Na2CO3溶液中含有的OH―数目为0.02NA
B.5.6gFe粉在0.1molCl2中充分燃烧,转移电子数为0.3NA
C.将100mL 1mol/LFeCl3溶液滴入沸水中,生成胶体粒子0.1NA
D.0.1molNa与O2反应生成Na2O和Na2O2时,转移电子数0.2NA
参考答案:A
本题解析:B项:反应中Cl2少量,应按Cl2的量算,转移电子数为0.2NA,故错;C项:反应为可逆反应,Fe3+不能全部转化为Fe(OH)3胶体,故错;D项:反应中Na元素的化合价升高了1价,因此转移电子数0.1NA,故错。故选A。
点评:题考查了阿伏伽德罗常数的应用,主要考查气体摩尔体积的应用,溶液体积的判断,氧化还原反应电子转移的计算,关键是过氧化钠是钠离子和过氧根离子构成,硫离子水解。
本题难度:一般
4、简答题 (1)下列配制100mL?0.100mol?L-1的碳酸钠溶液的操作步骤按先后顺序排列为______(填数字序号).
①将一定质量的碳酸钠置于小烧杯内,用少量水将其溶解
②待溶液冷至室温后,将其完全转移到容量瓶内,摇匀
③计算所需碳酸钠的质量,并用精密天平准确称取
④加水至容量瓶内,使凹液面最低点与容量瓶的刻度线相切,盖上塞子摇匀
⑤检查容量瓶是否渗漏
若量取20.00mL该碳酸钠溶液,应选用的量器是______.
(2)根据现有中学化学知识,判断下列有关实验叙述正确的是______(填序号).
A.检验红砖中氧化铁成分用到的试剂是盐酸和硫氰化钾溶液
B.用冰醋酸、蒸馏水和容量瓶等仪器配制pH为1的醋酸稀溶液
C.中和滴定时,酸式滴定管用蒸馏水清洗3次后,即加入标准盐酸溶液进行滴定
D.实验室用洁净的试管做银镜反应时不能将试管直接放酒精灯火焰上加热
E.由于碘在酒精中的溶解度大,所以可用酒精将碘水中的碘萃取出来.
参考答案:(1)因配制步骤有:检漏、计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,则操作顺序为⑤③①②④,因量筒的精确度为0.1ml,滴定管、移液管的精确度为0.01ml,所以量取20.00mL该碳酸钠溶液,应选用的量器是碱式滴定管或移液管,故答案为:⑤③①②④;碱式滴定管或移液管;
(2)A.因氧化铁与盐酸反应生成铁离子,滴加KSCN溶液变红色,故A正确;
B.因冰醋酸是弱酸,只能配制一定物质的量浓度的溶液,不能配制pH为1的醋酸稀溶液,故B错误;
C.根据中和滴定时,酸式滴定管用蒸馏水清洗3次后,然后加入标准盐酸溶液润洗,若直接加入标准盐酸溶液,会使盐酸溶液浓度降低,造成误差,故C错误;
D.实验室用洁净的试管做银镜反应时不能将试管直接放酒精灯火焰上加热,需水浴加热,故D正确;
E.虽碘在酒精中的溶解度大,但酒精易溶于水,所以不能萃取出碘,故E错误;
故选:AD.
本题解析:
本题难度:一般
5、选择题 甲、乙两烧杯中各盛有100mL 3mol・L―1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为V(甲):V(乙)=1:2,则加入铝粉的质量为(?)
A 5.4g ?B 3.6g ?C 2.7g ?D 1.6g
参考答案:A
本题解析:铝粉和盐酸反应方程式2Al+6HCl=2AlCl3+3H2,铝粉和NaOH反应方程式2Al+2NaOH+2H2O=2NaAlO2+3H2,根据方程式关系看到消耗等量的铝,需要盐酸的物质的量比NaOH多,但反应中V(甲):V(乙)=1:2,可知盐酸完全参与反应,根据H守恒,可知V(甲)=0.15mol,则V(乙)=0.3mol,对应方程式可知n(Al)=0.2mol,则加入铝粉的质量为5.4克,A正确。
本题难度:一般