1������� �����й����ʵ����ʺ����ʵ�Ӧ�þ���ȷ���ǣ�������
A��������Ũ������ʹ�������ۻ������ڳ�������������������Ũ����
B���������費���κ��ᷴӦ������ʯӢ������������
C���������Ⱦ��л�ԭ�ԣ�����������ˮ��ɱ������
D��ͭ�Ľ��������Ա������������ں��������װ����ͭ���Լ����丯ʴ
�ο��𰸣�A����Ũ�������ǿ�����ԣ��ܹ�������������Ӧ������������������Ҫ�����ۻ�����˳�����������������������Ũ���ᣬ��A��ȷ��
B�������������������ᷴӦ��SiO2 +4HF�TSiF4��+2H2O�����Բ�����ʯӢ����������������B����
C����������ȿ���������ˮ��ɱ����������Ϊ�����ǿ�����ԣ������ǻ�ԭ�ԣ���C����
D����Ҫ��������ĸ�ʴӦ���ӱ��������õĽ�������п�������������������������������D����
��ѡA��
���������
�����Ѷȣ�һ��
2��ѡ���� ����˵���������?
[? ]
A��Ǧ��о����Ҫԭ����ʯī����ͯ��ʹ��ʱ���������ж�
B��CO�ж�������ú¯�ľ��ҿɷ���������ˮ����������Ч������CO����ֹú���ж�
C������ˮ������ֲ����һ���ĵ���������CO2�Ļ��ͣ�������ֲ��Ĺ������
D������ᴿ��Ӧ�ã��ٽ��˰뵼��Ԫ���뼯��оƬҵ�ķ�չ������˵��������Ϣ���������Ĵ�����
�ο��𰸣�B
���������
�����Ѷȣ���
3��ѡ���� ��������֮���ת����һ����ʵ�ֵ��ǣ�������
A��Si��SiO2��H2SiO3��Na2SiO3
B��Al��Al2O3��Al��OH��3��NaAlO2
C��N2��NH3��NO��NO2��HNO3��NO2
D��S��SO3��H2SO4��SO2��Na2SO3��Na2SO4
�ο��𰸣�A���������費����ˮ��������ˮ��Ӧ������һ���õ����ᣬ��A����
B��Al2O3���������ᷴӦ����Al3+��Ȼ����Ӧ����Al��OH��3������һ��ʵ�֣���B����
C��������������Ӧ���ɰ�����������Ӧ����NO��NO����������Ӧ���ɶ�������������������ˮ��Ӧ�������ᣬŨ������ͭ��Ӧ�õ�������������C��ȷ��
D������������Ӧ���ɶ�����������������������Ӧ����������������ֱ�ӷ�Ӧ������������D����
��ѡC��
���������
�����Ѷȣ���
4��ѡ���� ���з�Ӧ����������������( ? )
A��������CO2ͨ��Na2SiO3��Һ��
B����AlCl3��Һ�еμ�ϡ��ˮ������
C��������CO2ͨ��BaCl2��Һ��
D����MgCl2��Һ�еμ�NaOH��Һ������
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5�������
�赥�ʼ��仯����Ӧ�÷�Χ�ܹ㡣��ش��������⣺
(1)�Ʊ���뵼����ϱ����ȵõ��ߴ��衣���ȼ���(SiHCl3)��ԭ���ǵ�ǰ�Ʊ��ߴ������Ҫ��������������ʾ��ͼ��ͼ
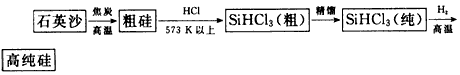
��д���ɴ�SiHCl3�Ʊ��ߴ���Ļ�ѧ����ʽ��__________________
�������Ʊ����̱����ϸ������ˮ������SiHCl3��ˮ���ҷ�Ӧ����H2SiO3��HCl����һ�����ʣ�д����ƽ��Ļ�ѧ����ʽ________________��H2��ԭSiHCl3������������O2����������ĺ����_____________��
(2)�����йع���ϵ�˵����ȷ����___________������ĸ����
A��̼���軯ѧ�����ȶ�����������������ˮ��
B��������Ӳ�ȴ��۵�ߣ����������������մɺ����
C���ߴ��ȵĶ���������������������ͨѶ����--���ά
D����ͨ�������ɴ��ʯ��ʯ��ʯӢ�Ƴɵģ����۵�ܸ�
E�����������跴Ӧ���ʲ�������Ϊ��Һ�ⵥ����
�ο��𰸣�(1)��SiHCl3+H2 Si+3HCl����SiHCl3+3H2O=H2SiO3��+3HCl��+H2����������������ϣ���������ը���������ܻ�����SiHCl3
Si+3HCl����SiHCl3+3H2O=H2SiO3��+3HCl��+H2����������������ϣ���������ը���������ܻ�����SiHCl3
(2)BC
���������
�����Ѷȣ�һ��