1、选择题 常温下,将pH=1的硫酸溶液平均分成两等份,一份加入适量水,另一份加入与该硫酸溶液物质的量浓度相同的氢氧化钠溶液,两者pH都升高了1,则加入的水和氢氧化钠溶液的体积比为( )
A.5:1
B.6: 1
C.10:1
D.11:1
参考答案:B
本题解析:设每份硫酸溶液体积都为V,每份溶液中c(H+)=0.1mol/L。
一份加水pH升高1,可得: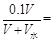 0.01;
0.01;
另一份加入与硫酸等浓度氢氧化钠溶液pH升高1,可得: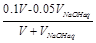 =0.01。
=0.01。
由以上二式解得水和氢氧化钠溶液体积比为6:1。
点评:pH=-lgc(H+)。
本题难度:简单
2、选择题 下列说法正确的是
[? ]
A.有些物质是由分子直接构成的,如二氧化碳、二氧化硅;有些物质是由原子直接构成,如金刚石、晶体硅;有些是由离子直接构成的,如氯化铵
B.分子是保持物质性质的一种微粒,且是化学变化中的最小微粒
C.在水溶液中能电离出自由移动离子的晶体不一定是离子晶体
D.使晶体中化学键断裂的变化一定是化学变化
参考答案:C
本题解析:
本题难度:简单
3、选择题 同种元素的原子一定具有
A.不同的质量数
B.相同的中子数
C.相同的质子数
D.不同的电子数
参考答案:AC
本题解析:同种元素的不同原子互为同位素,即质子数相同而中子数不同的同一元素的不同原子;又因质量数=质子数+中子数;所以正确选项为AC;
本题难度:一般
4、填空题 A、B、C为短周期元素,在周期表中所处位置如右图所示,A、C两种元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。
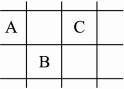
(1)写出A、B、C三种元素的名称:_____、_____、_____。
(2)B位于元素周期表中第_____周期,第_____族。
(3)C的原子结构示意图为_____,C的单质与水反应的化学方程式为_______________。
(4)比较B、C的原子半径_____,写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式____________________。
参考答案:(1)氮?硫?氟
(2)3?ⅥA
(3) 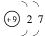 2F2+2H2O
2F2+2H2O 4HF+O2
4HF+O2
(4)r(S)>r(F)? 2NH3+H2SO4 (NH4)2SO4
(NH4)2SO4
本题解析:A、B、C为短周期(前三周期)元素,从A、B、C的相对位置看,A、C只能处在第2周期,而B为第3周期。
设A的原子序数为x-1,则C为x+1,B为x+8,则x-1+x+1=x+8,x=8
所以,A、B、C的原子序数分别为7、16、9,对应元素分别为N、S、F。
说明:元素的推断解题一要熟练、灵活运用规律;二要注意“特殊性”;三要运用相似性和递变性推测未学元素的某些性质;四要先划范围,再逐一排除。
本题难度:简单
5、选择题 A和M为两种元素,已知A位于短周期,且A2-与M+的电子数之差为8,则下列说法正确的是(?)
A.A和M原子的电子总数之和可能为11
B.A和M的原子序数之差为8
C.A和M原子的最外层电子数之和为8
D.A和M原子的最外层电子数之差为7
参考答案:A
本题解析:若A2-为O2-,则M+为Li+;若A2-为S2-,则M+为Na+。
本题难度:简单