1、选择题 下列装置或操作不能达到实验目的的是
[? ]
A. 利用排空气法收集CO2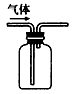
B. 实验室制取NH3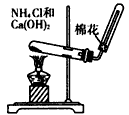
C. 实验室制取Fe(OH)2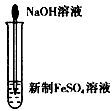
D. 实验室制乙酸乙酯 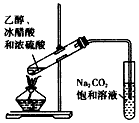
参考答案:D
本题解析:
本题难度:一般
2、简答题 某小组设计如图装置:可用于制取多种气体,也可用于验证物质的性质.
(1)关闭K2,打开K1时,可用装置I收集装置I所产生的气体,下列气体中能用此法收集的是:______.
A.O2 B.H2 C.NO D.SO2
写出实验室制备该气体的离子方程式:______.
上述另外几种气体中,若在装置Ⅱ中加满水,还不能制取和收集的是______.
若要收集该气体,改进的方法是______.
(2)利用I、Ⅲ装置比较物质的氧化性(K2打开,K1关闭):KMnO4>Cl2>Br2,在A中加浓盐酸时,应在B中加______,C中加______.C中的现象是______,装置Ⅲ中仪器D的作用是______.
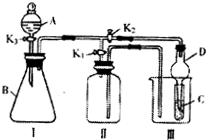
参考答案:(1)装置II中短管进气,为向下排空气法,SO2和O2的密度比空气大,应该用向上排空气法收集,NO能与空气中的氧气反应,所以NO不能用排气法收集,则能用向下排空气法收集的是氢气;
实验室用Zn与稀硫酸制备氢气,其反应的离子方程式为:Zn+2H+=Zn2++H2↑;
SO2易溶于水不能用排水法收集;SO2在饱和NaHSO3溶液中溶解度较小,所以SO2可以用排饱和NaHSO3溶液的方法收集,
故答案为:B; Zn+2H+=Zn2++H2;SO2;将I装置加满饱和NaHSO3溶液;
(2)依据实验装置图可知,A和B反应,生成产物通入C中反应,如证明氧化性:KMnO4>Cl2>Br2,需要根据氧化还原反应的氧化剂的氧化性大于氧化产物的规律分析判断,A为浓盐酸,滴入B中与高锰酸钾反应生成氯气,氯气通入C中与溴化钠溶液中反应生成溴单质,则C中溶液呈橙色;导气管下端连接球形干燥管,可以防倒吸;
故答案为:KMnO4固体;NaBr溶液;溶液呈橙色;防止倒吸.
本题解析:
本题难度:一般
3、选择题 下列装置或操作能达到实验目的的是
[? ]
A.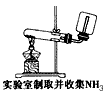
B.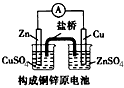
C.
D.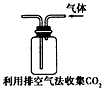
参考答案:C
本题解析:
本题难度:一般
4、选择题 某课外实验小组设计的下列实验不合理的是
[? ]
A.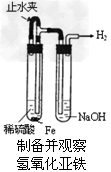
B.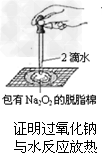
C.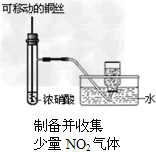
D.
参考答案:C
本题解析:
本题难度:一般
5、选择题 下列有关物质的性质及其解释都正确的是( )
A.在漂白粉中滴入70%的硫酸,立刻产生黄绿色气体,说明硫酸具有氧化性
B.不同的氨基酸在水溶液中形成晶体析出时pH各不相同,所以可以通过控制溶液pH的方法分离氨基酸
C.向一定体积的稀硝酸中加入过量的铜粉,生成的气体能被烧碱溶液完全吸收
D.在淀粉溶液中加入适量稀硫酸微热,再加少量新制氢氧化铜浊液加热,无红色沉淀,说明淀粉未水解
参考答案:B
本题解析:
本题难度:简单