1、选择题 氧化还原反应实际上包含氧化和还原两个过程。
(1)向氯酸钠的酸性水溶液中通入二氧化硫,该反应中氧化过程的反应式为:
SO2+2H2O - 2e- → SO42- + 4H+;
(2)向亚氯酸钠(NaClO2)固体中通入用空气稀释的氯气,该反应中还原过程的反应式为:
Cl2 + 2e- → 2Cl-。
在(1)和(2)反应中均会生成产物X,则X的化学式为
[? ]
A.NaClO
B.NaClO4
C.HClO
D.ClO2
参考答案:D
本题解析:
本题难度:简单
2、选择题 单晶硅是制作电子集成电路的基础材料。科学家预计,到2011年一个电脑芯片上将会集成10亿个晶体管,其功能远比我们想象的要大的多,这对硅的纯度要求很高。用化学方法可制得高纯度硅,其化学方程式为 : ①SiO2+2C Si+2CO ②Si+2Cl2
Si+2CO ②Si+2Cl2 SiCl4 ③SiCl4+2H2
SiCl4 ③SiCl4+2H2 Si+4HCl,其中反应①和③属于
Si+4HCl,其中反应①和③属于
[? ]
A.化合反应
B.分解反应
C.置换反应
D.复分解反应
参考答案:C
本题解析:
试题分析:
解:化合反应是两种或两种以上物质反应后生成一种物质的反应,其特点可总结为“多变一”;分解反应是一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”.置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物;复分解反应是指两种化合物相互交换成分生成两种化合物的反应。
由化学方程式可知,①③反应中的反应物和生成物都是一种单质和一种化合物,属于置换反应;②中的反应物是两种,生成物是一种,属于化合反应。
故选C.
本题难度:简单
3、选择题 下列对氧化还原反应所标出的电子转移情况中没有错误的是
[? ]
A. 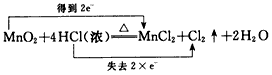
B. 
C. 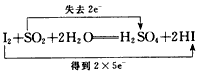
D. 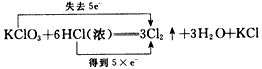
参考答案:A
本题解析:
本题难度:简单
4、选择题 下列反应中属于氧化还原反应的是?
[? ]
A.CaO+H2O=Ca(OH)2
B.SO2+2NaOH=Na2SO3+H2O?
C.CaCO3+2HCl==CaCl2+H2O+CO2↑?
D.?Cl2+2KI=2KCl+I2
参考答案:D
本题解析:
本题难度:简单
5、选择题 赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热有如下反应:Cu2S+2Cu2O=6Cu+SO2↑ 下列关于该反应的说法正确的是
A.Cu2S在反应中既是氧化剂,又是还原剂
B.Cu既是氧化产物,又是还原产物
C.该反应中氧化剂只有Cu2O
D.每生成19.2g Cu,反应中转移0.6mol电子
参考答案:A
本题解析:考查氧化还原反应的有关判断。根据反应的方程式可知,铜元素的化合价从+1价降低到0价,化合价降低,得到1个电子,因此Cu2S和Cu2O都是氧化剂,铜单质是还原产物;硫元素的化合价从-2价升高到+4价,失去电子,所Cu2S还是还原剂,SO2是氧化产物,所以只有选项A是正确的,其余都是错误的,选项D中19.2g铜的物质的量是0.3mol,转移电子的物质的量是0.3mol,答案选A。
本题难度:一般