1、选择题 下列物质溶于水,不发生氧化还原反应的是
A.NO2溶于水
B.Na2O2溶于水
C.Cl2溶于水
D.CaO溶于水
参考答案:D
本题解析:分析:A.反应生成硝酸和NO;
B.反应生成氢氧化钠和氧气;
C.反应生成盐酸和HClO;
D.反应生成氢氧化钙.
解答:A.反应生成硝酸和NO,N元素的化合价升高、降低,发生氧化还原反应,故A不选;
B.反应生成氢氧化钠和氧气,O元素的化合价升高、降低,发生氧化还原反应,故B不选;
C.反应生成盐酸和HClO,Cl元素的化合价升高、降低,发生氧化还原反应,故C不选;
D.反应生成氢氧化钙,没有元素的化合价变化,则不发生氧化还原反应,故D选;
故选D.
点评:本题考查氧化还原反应,明确发生的化学反应及反应中元素的化合价变化即可解答,注意物质性质的考查,题目难度不大.
本题难度:一般
2、选择题 M、N、X、Y均为常见的物质,它们之间有如下转化关系(反应条件和其它产物已略去):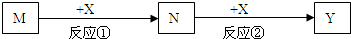
下列选项符合的是
A.M:N2,X:O2
B.M:Al,X:NaOH
C.M:Fe,X:Cu2+
D.M:Ca(OH)2,X:Na2CO3
参考答案:A
本题解析:分析:依据转化关系的特征是M和X能反应两部连续反应说明变化过程中存在变价元素的物质,结合选项中的物质进行分别推断.
解答:A、M:N2,X:O2 存在转化关系:N2 NO
NO NO2;符合转化关系,故A正确;
NO2;符合转化关系,故A正确;
B、M:Al,X:NaOH存在转化关系:Al NaAlO2,不能继续和氢氧化钠溶液反应,故B错误;
NaAlO2,不能继续和氢氧化钠溶液反应,故B错误;
C、Fe,X:Cu2+存在转化关系:Fe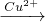 Fe2+,不能继续和铜离子溶液反应,故C错误;
Fe2+,不能继续和铜离子溶液反应,故C错误;
D、Ca(OH)2,X:Na2CO3存在转化关系:Ca(OH)2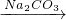 CaCO3,不能继续反应,故D错误;
CaCO3,不能继续反应,故D错误;
故选A.
点评:本题考查了物质转化关系的应用,物质性质的应用,主要考查镁、铝、铁氢氧化钙等物质的性质应用,较简单.
本题难度:困难
3、选择题 由CO、H2和O2组成的混合气体,在一定条件下恰好完全反应,测得生成物在101?kPa、120℃下对空气的相对密度为1.293,则原混合气体中CO所占体积分数为
A.1/3
B.2/3
C.1/2
D.1/6
参考答案:C
本题解析:
本题难度:一般
4、选择题 下列物质中,常温下呈液态的是
A.I2
B.MgCl2
C.Br2
D.SO2
参考答案:C
本题解析:分析:I2和MgCl2在常温下呈固态,Br2为液态,SO2为气态.
解答:A.I2在常温下呈固态,为紫色固体,故A不选;
B.MgCl2在常温下呈固态,为无色固体,故B不选;
C.在常温下,Br2为红棕色液体,故C选;
D.在常温下,SO2为无色气体,故D不选.
故选C.
点评:本题考查常见物质的物理性质,题目难度不大,注意常见元素化合物的性质,注重相关基础知识的积累.
本题难度:一般
5、选择题 碳与浓硝酸反应,显示了浓硝酸的
A.不稳定性
B.挥发性
C.强氧化性
D.酸性
参考答案:C
本题解析:浓硝酸可将碳氧化成二氧化碳,体现其氧化性
本题难度:简单