1、选择题 下列说法正确的是( )
A.吸热反应一定是反应物能量低于生成物能量
B.由于燃料的燃烧是一次性的,所以燃料电池属于一次电池
C.电能是经过一次能源加工转换得到的能源,因此,属于二次能源
D.断开旧化学键与形成新化学键之间的能量差只能以热量的形式释放
参考答案:A、若反应中生成物总能量高于反应物总能量,反应是一个吸热反应,反之是一个放热反应,故A错误;
B、因燃料电池只要补充燃料、氧化剂可重复使用,故B错误;
C、因二次能源是经过一次能源加工转换得到的能源,故C正确;
D、因化学反应中能量可以以热能、光能等形式释放出去,故D错误;
故选:C.
本题解析:
本题难度:简单
2、填空题 已知;①Fe(s)+CO2(g)
 FeO(s)+CO(g) ΔH=a kJ・mol-1,平衡常数为K;
FeO(s)+CO(g) ΔH=a kJ・mol-1,平衡常数为K;
②Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH=b kJ・mol-1。
测得在不同温度下,K值如下:
温度/℃
| 500
| 700
| 900
|
K
| 1.00
| 1.47
| 2.40
|
(1)反应①为__________(选填“吸热”或“放热”)反应。
(2)若500 ℃时进行反应①,CO2的起始浓度为2 mol・L-1,CO的平衡浓度为?。
(3)下列关于反应①的说法正确的是?。
A.达到平衡后保持其他条件不变,升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动
B. 在500 ℃下反应,当c(CO2)=c(CO)时,反应达到平衡状态
C.恒温恒容下,当容器内气体密度不再变化时,反应达到平衡状态
D.加压、升温和使用催化剂均可增大反应物的转化率
(4)由已知反应,写出Fe2O3(s)被CO(g)还原成FeO(s)的热化学方程式?。
(5)室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为2.7时,Fe3+开始沉淀;当溶液pH为4时,c(Fe3+)=__________mol・L-1(已知:Ksp[Fe(OH)3]=4.0×10-36)。
(6)新型锌空电池与锂电池相比,具有能量密度高、安全性好且成本低。该电池的总反应为2Zn+O2===2ZnO,电解质溶液为KOH溶液,则负极的电极反应式为_______。
若以该电池为电源,用惰性电极电解硫酸铜溶液,为保证阴极有6.4g铜析出,理论上至少需要标准状况下 ?L空气(空气中含氧气按20%计算)进入该电池。
参考答案:(1)吸热?(2)1.00 mol・L-1?(3)B C(对一个计1分)
(4) Fe2O3(s)+CO(g)== 2FeO(s)+CO2(g) ΔH=(2a+b) kJ・mol-1
(5)4.0×10-8
(6)Zn - 2e-+2OH--== ZnO+H2O? 5.60
本题解析:(1)反应①平衡常数为K随温度的升高而增大,说明是吸热反应;
(2) 500℃时进行反应①的K=1,平衡时c(CO)=c(CO2);CO2的起始浓度为2 mol・L-1,CO的平衡浓度为1 mol・L-1。
(3)反应Fe(s)+CO2(g)
 FeO(s)+CO(g) ΔH<0,
FeO(s)+CO(g) ΔH<0,
A.达到平衡后保持其他条件不变,升高温度,正反应速率增大,逆反应速率也增大,不会减小,故不正确;
B. 在500 ℃下反应K=1,故当c(CO2)=c(CO)时,反应达到平衡状态
C.恒温恒容下,气体的物质的量不变,但CO生成CO2,质量增重,正向移动,当容器内气体密度不再变化时,反应达到平衡状态,正确;
D.加压和使用催化剂不会使平衡移动,故反应物的转化率不变,不正确。
(4)根据盖斯定律来写。
(5)pH=4时,c(OH-)=10-10mol・L-1,c(Fe3+)=  ?=4.0×10-6mol・L-1
?=4.0×10-6mol・L-1
(6)电池的负极是活泼金属Zn,注意碱性环境得出负极反应式:Zn-2e-+2OH-==ZnO+H2O,
根据电子得失2Cu――O2,6.4g铜需要0.05molO2,0.25mol(0.25 mol×22.4L/mol =5.60L)空气。
本题难度:一般
3、选择题 下列离子方程式正确的是(? )
A.碳酸氢铵溶液与足量氢氧化钠溶液反应: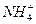 +OH-====NH3・H2O
+OH-====NH3・H2O
B.Fe(OH)3与氢碘酸溶液混合:Fe(OH)3+3H+====Fe3++3H2O
C.电解精炼铜的阴极反应是:Cu2++2e-====Cu
D.1 mol・L-1的NaAlO2溶液和2.5 mol・L-1的HCl等体积互相均匀混合:2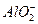 +5H+====Al(OH)3↓+Al3++H2O
+5H+====Al(OH)3↓+Al3++H2O
参考答案:CD
本题解析:A项中,NaOH足量,应放出NH3,A项错。B项中,Fe3+与I-不能共存。C项正确。D项由于HCl过量,故产物有Al(OH)3,也有Al3+,正确。
本题难度:简单
4、选择题 下列叙述正确的是( )
A.伴随着能量的变化过程,就是发生化学反应的过程
B.物质燃烧一定是放热反应
C.放热的化学反应不需要加热就能发生
D.吸热反应不加热就不会发生
参考答案:A、物理过程也可能伴随能量变化,如有的物质溶解时会放出能量,所以伴随着能量的变化过程,不一定是发生化学反应的过程,故A错误;
B、物质燃烧都会放出能量,所以物质燃烧一定是放热反应,故B正确;
C、放热反应有的也需要反应条件,如碳的燃烧需要点燃,故C错误;
D、有的吸热反应常温下也能发生,如碳酸氢铵分解是吸热反应,但常温下能发生,故D错误;
故选B.
本题解析:
本题难度:简单
5、选择题 下列对化学反应的认识,错误的是?( )
A.会引起化学键的变化
B.会产生新物质
C.必然引起物质状态的变化
D.必然伴随着能量的变化
参考答案:A.化学反应必定会引起化学键的变化,故A正确;
B.化学变化是指有新物质生成的变化,会产生新物质,故B正确;
C.化学反应不一定引起物质状态的变化,如氢气与氯气反应生成氯化氢,都是气体,故C错误;
D.化学反应必然伴随着能量的变化,故D正确.
故选C.
本题解析:
本题难度:简单