1��ѡ���� ����˵������ȷ����
[? ]
A������FeCl2��Һʱ���ɽ�FeCl2����������Ũ���ᣬ�ټ�ˮϡ�ͺ�������м����
B�����ܵ���Ϊ��ֹ����汻��ʴӦͿ�ϸ�ˮ���ϲ������Դ��������
C��pHֵ��Ϊ9��NaOH��Һ��Na2CO3��Һ������Һ��ˮ�ĵ���̶���ͬ
D��0.1mol/L?����HA��Һ��0.05mol/L?NaOH��Һ�������Ϻ�������Һ��Ũ�ȼ��У�
2c(H+)+c(HA)?=?c(A��)+2?c(OH��)
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ѡ���� ������Һ�У����ӵ����ʵ���Ũ�ȹ�ϵ��ȷ����
[? ]
A��0.1?mol/L?Na2CO3��Һ��c(Na��)��2c(H2CO3)��2c(HCO3��)��2c(CO32��)
B��0.1?mol/L?NH4Cl��Һ��c(NH4��)��c(Cl��)
C�����������Һ�м����������ᣬ�õ������Ի����Һ��c(Na��)>c(CH3COO��)>c(H��)>c(OH��)
D������������Һ�еμ�ϡ����õ���pH��5�Ļ����Һ��c(Na��)��c(NO3��)
�ο��𰸣�AD
���������
�����Ѷȣ�һ��
3��ѡ���� �����£���0.1000 mol��L-1 NaOH��Һ�ζ�20.00 mL 0.1000 mol��L-1 CH3COOH��Һ���õζ�������ͼ������˵����ȷ����
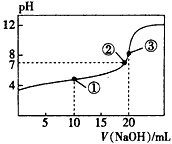
[? ]
A.�����ʾ��Һ�У�c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
B.�����ʾ��Һ�У�c(Na+)=c(CH3COOH)+c(CH3COO-)
C.�����ʾ��Һ�У�c(Na+)��c(OH-)��c(CH3COO-)>c(H+)
D.�ζ������п��ܳ��֣�c(CH3COOH)��c(CH3COO-)>c(H+)��c(Na+)>c(OH-)
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� ��1��ˮ�ĵ���ƽ��������ͼ��ʾ����A���ʾ25��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ�B���ʾ100��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȡ�100��ʱ1?mol��L��1?��NaOH��Һ�У���ˮ�������c��H+����_______mol/L�� Kw��25�棩______Kw��100�棩�������������������֮һ����
��2��25��ʱ����ˮ�ĵ���ƽ����ϵ�м�������NH4Cl���壬��ˮ�ĵ���ƽ���Ӱ����__________����ٽ��������ơ���Ӱ�족֮һ����

��3������ƽ�ⳣ���Ǻ���������ʵ���̶�ǿ��������������֪

��25��ʱ,�е�Ũ�ȵ�NaCN��Һ��Na2CO3��Һ��CH3COONa��Һ������Һ��pH�ɴ�С��˳��Ϊ_____________________��
��25��ʱ,��Ũ�ȵ�CH3COOH��Һ��NaOH��Һ�������ϣ�������Һ�Լ��ԣ��� c(Na��)_______?c(CH3COO��)�������������������֮һ����
����NaCN��Һ��ͨ������CO2����������Ӧ�Ļ�ѧ����ʽΪ___________________?��
�ο��𰸣���1��1��10-12����
��2���ٽ�
��3����Na2CO3��Һ��pH��NaCN��Һ��pH��CH3COONa��Һ��pH���ڣ�����NaCN��H2O��CO2��HCN��NaHCO3
���������
�����Ѷȣ�һ��
5��ѡ���� ����ˮ��Һ�����Ե��ǣ�������
A����������Һ
B��̼��������Һ
C��̼������Һ
D���Ȼ�����Һ
�ο��𰸣�D
���������
�����Ѷȣ�һ��