1、选择题 在恒容密闭器中通入物质的量浓度均0.1 mol・L-1的CH4与CO2,在一定条件下发生反应:CO2(g)+CH4(g) 2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如下图,下列有关说法一定正确的是(?)
2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如下图,下列有关说法一定正确的是(?)
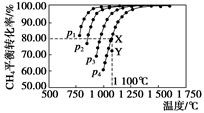
A.上述反应的ΔH>0
B.压强p1>p2>p3>p4
C.1 100 ℃该反应的平衡常数为64
D.压强为p4时,在Y点:v(正)<v(逆)
参考答案:A
本题解析:A项,温度越高,转化率越大,升温平衡右移,ΔH>0,正确;B项,增大压强,平衡左移,CH4的转化率减小,所以p4>p3>p2>p1,错误;C项,CO2(g)+CH4(g)=2CO(g)+2H2(g)
起始/mol・L-1? 0.1? 0.1? 0? 0
平衡/mol・L-1? 0.1-x? 0.1-x? 2x? 2x
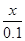 ×100%=80%
×100%=80%
x=0.08
K=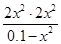 =1.638 4,错误;D项,Y点未达平衡,若要达平衡,CH4的转化率应增大,所以v(正)>v(逆)。
=1.638 4,错误;D项,Y点未达平衡,若要达平衡,CH4的转化率应增大,所以v(正)>v(逆)。
本题难度:一般
2、填空题 (8分)在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为
C分别在三种不同实验条件下进行,它们的起始浓度均为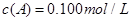 、
、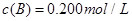 及
及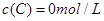 。反应物A的浓度随时间的变化如下图所示。
。反应物A的浓度随时间的变化如下图所示。
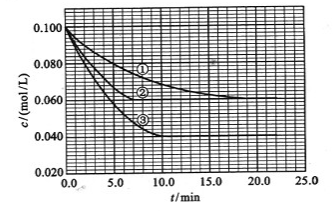
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②__________?_____;
③__________?_____;
(2)实验②平衡时B的转化率为_________;实验③平衡时C的浓度为____________。
参考答案:(1)②加催化剂;达到平衡的时间缩短,平衡时A的浓度未变
③温度升高;达到平衡的时间缩短,平衡时A的浓度减小
(2)40%(或0.4);0.06mol/L;
本题解析:(1)①和②比较,平衡时A的浓度相同,但②反应速率快,可能使用了催化剂;①和③比较,③反应速率快且平衡时A浓度小,因起始时两种条件下各物质的浓度均相同,所以不可能是浓度因素使速率加快。反应是在溶液中进行的反应,压强对反应影响不大,所以只能是温度升高,使反应速率加快。
(2)实验②起始时A的浓度为0.1mol/L,平衡时A的浓度为0.06mol/L,所以消耗的A的浓度为0.04mol/L,消耗的B的浓度为0.08mol/L,B的转化率为0.08/0.2=0.4;实验②起始时A的浓度为0.1mol/L,平衡时A的浓度为0.04mol/L,消耗A的浓度为0.06mol/L,生成C的浓度为0.06mol/L。
点评:影响反应速率的因素通常有浓度、温度、压强、催化剂,要学会从图像中寻找化学反应速率变化的因素。
本题难度:一般
3、填空题 (8分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g)  ?2NO2(g)体系中,n(NO)随时间的变化如表:
?2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s)
| 0
| 1
| 2
| 3
| 4
| 5
|
n(NO)(mol)
| 0.020
| 0.010
| 0.008
| 0.007
| 0.007
| 0.007
|
(1)写出该反应的平衡常数表达式:K=?。已知: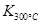 >
>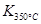 ,则该反应是?热反应。
,则该反应是?热反应。
(2)右图中表示NO2的变化的曲线是?。用O2表示从0~2 s内该反应的平均速率v=?。

(3)能说明该反应已达到平衡 状态的是?
状态的是? ?。
?。
a. v(NO2)=2v(O2) ? b.容器内压强保持不变
c.v逆 (NO)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动是?。
a.及时分离除NO2气体? b.适当升高温度
c.增大O2的浓度? d.选择高效催化剂
参考答案:

本题解析:略
本题难度:一般
4、选择题 向新制备的氯水中不断滴入饱和NaCl溶液,则下列曲线符合氯水pH变化的是(? )
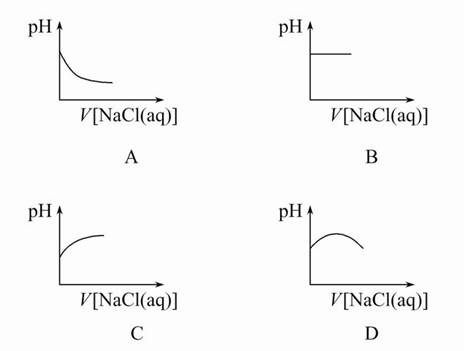
参考答案:C
本题解析:新制氯水中存在的主要平衡是Cl2+H2O H++Cl-+HClO,当加入饱和NaCl溶液时,c(Cl-)增大,使平衡逆向移动,c(H+)减小。
H++Cl-+HClO,当加入饱和NaCl溶液时,c(Cl-)增大,使平衡逆向移动,c(H+)减小。
本题难度:一般
5、选择题 下列图示与对应的叙述相符的是

A.由图甲可以判断:若T1>T2,反应A(g)+ B(g) 2C(g)的△H<0
2C(g)的△H<0
B.图乙表示压强对可逆反应2A(g)+2 B(g) 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C.根据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH溶液,调节pH≈4
D.图丁表示用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,溶液pH随加入盐酸体积的变化
参考答案:A
本题解析:A、若T1>T2,温度升高A的转化率降低,说明升高温度平衡逆向移动,则正向是放热反应,△H<0,正确;B、图乙表示是否使用催化剂,因为到达平衡的时间改变而反应物的百分含量不变,说明平衡不移动,所以乙代表使用了催化剂,错误;C、调节溶液的pH=4,溶液呈酸性,若加入氢氧化钠溶液,则溶液呈碱性,铜离子也会沉淀,错误;D、用盐酸滴定氢氧化钠溶液,开始的pH是氢氧化钠溶液的pH值,应大于7,错误,答案选A。
本题难度:一般