1、选择题 已知:NO+NO2+2NaOH====2NaNO2+H2O,2NO2+2NaOH====NaNO3+NaNO2
+H2O。NO和NO2的混合气体的组成可表示为NOx。该混合气体通入NaOH溶液被完全吸收时,x的值为(?)
A.x≤1.5
B.x="3.5"
C.x="1.2"
D.x≥1.5
参考答案:D
本题解析:由题中所给反应过程可知,要使混合气体通入NaOH溶液被完全吸收,则NO2与NO的物质的量比应大于等于1,即n(NO2)/n(NO)≥1。当n(NO2)/n(NO)=1时,混合气体中所含NO2和NO的物质的量相等,此时x=1.5,若要n(NO2)/n(NO)>1,须x>1.5,故x应满足的条件是x≥1.5。
本题难度:简单
2、选择题 某氮的氧化物和一氧化碳在催化剂的作用下充分反应,生成氮气和二氧化碳。若测得氮气和二氧化碳的物质的量之比为1∶2,该氮的氧化物是?
A.N2O
B.NO
C.NO2
D.N2O5
参考答案:B
本题解析:从反应产物N2和CO2的系数之比为1∶2得出参加反应的氮的氧化物NOx和CO的系数之比为2∶2,即:2NOx+2CO→N2+2CO2,由氧原子守恒可知x=1,即NO。
本题难度:一般
3、计算题 把19.2 g的Cu放入足量的稀硝酸中,微热至Cu完全反应。
已知:3Cu + 8HNO3(稀) = 3Cu(NO3)2 +2NO↑+ 4H2O求:
(1)参加反应的硝酸的物质的量;
(2)被还原的硝酸的质量;
(3)生成的NO在标准状况下的体积。
参考答案:(1)0.8mol;(2)12.6g; (3)4.48L。
本题解析:(1)19.2g铜的物质的量是19.2g÷64g/mol=0.3mol
所以依据化学方程式可知
参加反应的硝酸的物质的量为: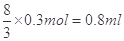
(2)铜在反应中失去电子0.3mol×2=0.6mol,根据方程式可知,氮元素的化合价从+5价降低到+2价,得到3个电子实验根据电子的得失守恒可知,被还原的硝酸的物质的量是0.6mol÷3=0.2mol,质量是0.2mol×63g/mol=12.6g。
(3)被还原的硝酸的物质的量是0.2mol,则根据氮原子守恒可知,生成的NO的物质的量是0.2mol,则在标准状况下的体积是0.2mol×22.4L/mol=4.48L
本题难度:一般
4、选择题 下列事实或名词与环境污染无关的是(?)
A.温室效应
B.酸雨
C.光化学烟雾
D.潮汐
参考答案:D
本题解析:CO2过多引起温室效应,S、N氧化物的过量排放引起酸雨,而潮汐与环境污染无关。
本题难度:简单
5、选择题 相同状况下,在体积相同的三个烧瓶中分别盛NH3、HCl和NO2气体,并分别倒立在水槽里,充分溶解后烧瓶内三种溶液物质的量浓度之比为(设烧瓶内液体未扩散到水槽里)( )
A.1∶1∶1
B.2∶2∶3
C.3∶3∶2
D.2∶2∶1
参考答案:A
本题解析:盛三种气体的烧瓶倒置在水中,气体减少的体积和进入烧瓶中溶液的体积都满足相等,所得溶液的物质的量浓度均相等。
本题难度:简单