|
高中化学知识点大全《绿色化学》在线测试(2019年最新版)(十)
2019-06-28 21:08:24
【 大 中 小】
|
1、填空题 I.目前,我国采用“接触法”制硫酸,设备如图所示:
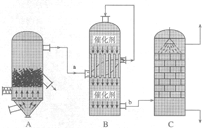
(1)图中设备A的名称是_____________,该设备中主要反应的化学方程式为 ?。
(2)有关接触法制硫酸的下列说法中,不正确的是_____(填字母序号)。
A.二氧化硫的接触氧化在接触室中发生
B.吸收塔用浓度为98.3%浓硫酸吸收三氧化硫
C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失2%
D.B装置中反应的条件之一为较高温度是为了提高SO2的转化率
| E.硫酸工业中在接触室安装热交换器是为了利用SO3转化为 H2SO4时放出的热量
II.纯碱是一种重要的化工原料。制碱工业主要有“氨碱法”(索尔维法)和“联合制碱法”(侯氏制碱法)两种工艺。请按要求回答问题:
(3)CO2是制碱工业的重要原料,“联合制碱法”中CO2的来源于??,“氨碱法”中CO2来源于??。
(4)氨碱法的原子利用率(原子利用率=期望产物的总质量与生成物的总质量之比) ?。
(5)写出“联合制碱法”有关反应的化学方程式:?。
参考答案:Ⅰ.(1)沸腾炉 ?4FeS2 +11O2 ?2Fe2O3 + 8SO2 ?(2)D、E ?2Fe2O3 + 8SO2 ?(2)D、E
Ⅱ.(3)合成氨厂?煅烧石灰石?(4)0.49 (106/217)
(5)NH3 + H2O + CO2 + NaCl(饱和)= NaHCO3 ↓+ NH4Cl
2NaHCO3 Na2CO3 + CO2↑+ H2O Na2CO3 + CO2↑+ H2O
本题解析:Ⅰ.(1) “接触法”制硫酸设备A的名称是沸腾炉;设备B的名称是接触室;设备C的名称是吸收塔。在设备A中主要反应的化学方程式为4FeS2 +11O2 ?2Fe2O3 + 8SO2。(2)A.在接触室中发生反应:2SO2+O2 ?2Fe2O3 + 8SO2。(2)A.在接触室中发生反应:2SO2+O2 2SO3因此该选项正确。B.如果用水吸收SO3,容易形成酸雾,不利于SO3的吸收。所以在吸收塔中一般是用98.3%浓硫酸吸收三氧化硫形成发烟硫酸,然后再稀释成所需要的浓度。正确。C.C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则其中各组分的损失也都是2%.这与物质的组成无关。正确。D.在设备B中发生的反应2SO2+O2 2SO3因此该选项正确。B.如果用水吸收SO3,容易形成酸雾,不利于SO3的吸收。所以在吸收塔中一般是用98.3%浓硫酸吸收三氧化硫形成发烟硫酸,然后再稀释成所需要的浓度。正确。C.C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则其中各组分的损失也都是2%.这与物质的组成无关。正确。D.在设备B中发生的反应2SO2+O2 2SO3为放热反应,如果升高温度,根据平衡移动原理,升高温度,化学平衡会向吸热反应方向移动,对该反应来说就是向逆反应方向移动。这对于提高SO2的转化率不利。之所以采用较高的温度,是为了加快化学反应速率,缩短达到平衡所需要的时间。提高生产效率。错误。E.硫酸工业中在接触室安装热交换器是为了利用SO2氧化为SO3时的热量。错误。Ⅱ.(3)“联合制碱法”中CO2的来源于合成氨厂;“氨碱法”中CO2来源于煅烧石灰石。(4)氨碱法的化学反应原理为:NH3+CO2+H2O==NH4HCO3;NaCl+NH4HCO3==NaHCO3↓+NH4Cl?2NaHCO3 2SO3为放热反应,如果升高温度,根据平衡移动原理,升高温度,化学平衡会向吸热反应方向移动,对该反应来说就是向逆反应方向移动。这对于提高SO2的转化率不利。之所以采用较高的温度,是为了加快化学反应速率,缩短达到平衡所需要的时间。提高生产效率。错误。E.硫酸工业中在接触室安装热交换器是为了利用SO2氧化为SO3时的热量。错误。Ⅱ.(3)“联合制碱法”中CO2的来源于合成氨厂;“氨碱法”中CO2来源于煅烧石灰石。(4)氨碱法的化学反应原理为:NH3+CO2+H2O==NH4HCO3;NaCl+NH4HCO3==NaHCO3↓+NH4Cl?2NaHCO3 Na2CO3 + CO2↑+ H2O ;2NH4Cl+Ca(OH)2 Na2CO3 + CO2↑+ H2O ;2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O。CO2、NH3循环利用。在该方法中,目标产物为Na2CO3;实际产物为Na2CO3和CaCl2。所以原子利用率为[106÷(106+111)]×100%=49%(或106/217)。(5) “联合制碱法”有关反应的化学方程式为NH3 + H2O + CO2 + NaCl(饱和)= NaHCO3 ↓+ NH4Cl; 2NaHCO3 CaCl2+2NH3↑+2H2O。CO2、NH3循环利用。在该方法中,目标产物为Na2CO3;实际产物为Na2CO3和CaCl2。所以原子利用率为[106÷(106+111)]×100%=49%(或106/217)。(5) “联合制碱法”有关反应的化学方程式为NH3 + H2O + CO2 + NaCl(饱和)= NaHCO3 ↓+ NH4Cl; 2NaHCO3 ?Na2CO3 + CO2↑+ H2O。 ?Na2CO3 + CO2↑+ H2O。
本题难度:一般
2、选择题 从降低成本和减少环境污染的角度考虑,制取硝酸铜最好的方法是
[? ]
A.铜和浓硝酸反应
B.铜和稀硝酸反应
C.氧化铜和硝酸反应
D.氯化铜和硝酸银反应
参考答案:C
本题解析:
本题难度:简单
3、填空题 (8分)将肥皂液分装在两支试管中,向第一支试管中加入稀硫酸,有____________产生,向第二支试管中加入MgCl2溶液,则产生____________,有关反应的离子方程式为:_____________________________________,_____________________________________。
参考答案:白色沉淀 白色沉淀
C17H35COO-+H+====C17H35COOH↓?2C17H35COO-+Mg2+====Mg(C17H35COO)2↓
本题解析:肥皂的主要成分是高级脂肪酸钠,加入稀硫酸,生成不溶于水的高级脂肪酸沉淀,加入氯化镁溶液,产生不溶于水的高级脂肪酸镁沉淀。?
本题难度:简单
4、选择题 下列石油产品加工过程中可以得到大量芳香烃的是
A.减压分馏
B.重油裂解
C.催化重整
D.干馏
参考答案:C
本题解析:A错,石油的减压分馏得到的是以烷烃为主的混合物;
B错,重油裂解得到烷烃和烯烃的混合物,主要得到的是乙烯、丙烯、甲烷等含碳原子数的烃。
C正确,石油的催化重整是获得芳香烃的途径之一,芳香烃还可以从煤焦中得到。
D错,干馏是指,将煤隔绝空气加强热使之分解的过程。
本题难度:一般
5、填空题 (共6分)瑞典皇家 科学院宣布,将2007年诺贝尔化学奖授予德国马普学会弗里茨-哈伯(Fritz-Haber)研究所的格哈德・埃特尔(Gerhard Ertl)教授,以表彰他在固体表面化学过程研究领域作出的开拓性成就。合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3。 科学院宣布,将2007年诺贝尔化学奖授予德国马普学会弗里茨-哈伯(Fritz-Haber)研究所的格哈德・埃特尔(Gerhard Ertl)教授,以表彰他在固体表面化学过程研究领域作出的开拓性成就。合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4:5,其中Fe2+与Fe3+物质的量之比为_________。
(2)当催化剂中Fe2+与Fe3+物质的量之比为1:2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为_________(用小数表示)。
(3)以Fe2O3为原料制备上述催化剂,可向其中加入适量碳粉,发生如下反应:
2Fe2O3 +C  =4FeO +CO2↑,为制得这种催化活性最高的催化剂,应向480g Fe2O3粉末中加入碳粉的质量为_________ g。 =4FeO +CO2↑,为制得这种催化活性最高的催化剂,应向480g Fe2O3粉末中加入碳粉的质量为_________ g。
参考答案:(1)1:1 (2分)
(2)0.724?(2分)
(3)6g(2分)
本题解析:略
本题难度:简单
|