|
�߿���ѧ֪ʶ���ܽᡶԭ���ԭ��������ǿ����ϰ��2019�����°棩(ʮ)
2019-06-28 21:09:46
�� �� �� ��
|
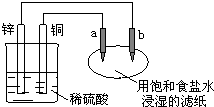
1��ѡ���� ��ͼ��ʾ��a��b������ʯī��������������ȷ���ǣ�������
A��ϡ����pH����
B������ʳ��ˮpH��С
C��a��������������ԭ��Ӧ
D������ֽ�ϵμӷ�̪��Һ��a��������ɫ���
| 
�ο��𰸣�A
���������
�����Ѷȣ���
2������� ��ͼ��һ����ѧ���̵�ʾ��ͼ����֪�׳ص��ܷ�ӦʽΪ��2CH3OH+3O2+4KOH�T2K2CO3+6H2O
��1����ش����е缫�����ƣ�B��ʯī���缫��������______��
��2��д���缫��Ӧʽ��
ͨ��O2�ĵ缫�ĵ缫��Ӧʽ��______��
A��Fe���缫�ĵ缫��ӦʽΪ______��
��3���ҳ��з�Ӧ�Ļ�ѧ����ʽΪ______��
��4�����ҳ���A��Fe��������������5.40gʱ���׳�������������O2______mL����״���£�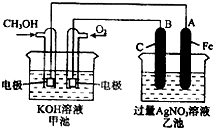
�ο��𰸣���1�����ݷ�Ӧ����ʽ֪����װ����һ��ȼ�ϵ�أ����Լ��ǰѻ�ѧ��ת��Ϊ���ܵ�װ�ã���ԭ��أ�������ӵ�Դ�������ǵ��أ�����2CH3OH+3O2+4KOH=2K2CO3+6H2O֪��CH3OH����������Ӧ�����Ըõ缫�Ǹ�����O2 ������ԭ��Ӧ�����Ըõ缫��������ʯī��ԭ��ص���������������Bʯī�缫��������
�ʴ�Ϊ��������
��2������2CH3OH+3O2+4KOH=2K2CO3+6H2O֪��CH3OH����������Ӧ�����Ըõ缫�Ǹ�����O2 �õ��Ӻ�ˮ��Ӧ�������������ӣ�������ԭ��Ӧ�����Ըõ缫��������ʯī��ԭ��ص���������������ʯī�缫�������õ缫�Ϸ���������Ӧ���缫��ӦΪ��O2+2H2O+4e-=4OH-�����缫���������õ缫�������ӵõ��ӷ�����ԭ��Ӧ���缫��ӦΪ��4Ag++4e-=4Ag��
�ʴ�Ϊ��O2+2H2O+4e-=4OH-��4Ag++4e-=4Ag��
��3���ҳ������ӷŵ�˳��Ϊ�������� Ag+��H+��������OH-��NO3 -�������缫��ӦΪ��O2+2H2O+4e-=4OH-�������缫��ӦΪ��4Ag++4e-=4Ag�����ݵ����غ�͵���ʵ��д����ѧ����ʽ��4AgNO4+2H2O ?ͨ��?.?4Ag+O2��+4HNO3
�ʴ�Ϊ��4AgNO4+2H2O ?ͨ��?.?4Ag+O2��+4HNO3��
��4���ҳ���A��Fe��������������������������5.40g���������ݵ�ʧ��������ȣ����������Ĺ�ϵʽΪ��
O2--------4Ag
22.4L �� 4��108 ��g
280mL? 5.40g
�ʴ�Ϊ��280��
���������
�����Ѷȣ�һ��
3��ѡ���� �£�N2H4��������ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20%��30%��KOH��Һ������˵���У�����ȷ����
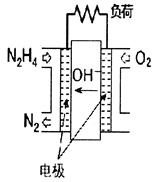
A���õ�طŵ�ʱ��ͨ���µ�һ��Ϊ����
B�����ÿ�ͷ�1mol N2ת�Ƶĵ�����Ϊ4NA
C��ͨ�������һ���ĵ缫��Ӧʽ�ǣ�O2+2H2O+4e��=4OH��
D����ع���һ��ʱ��������Һ��pH������
�ο��𰸣�D
���������ԭ����и���ʧȥ���ӣ��������ڸ���ͨ�룬A��ȷ�����е�Ԫ�صĻ��ϼ��ǣ�2�ۣ����������ǵ���������ÿ�ͷ�1mol N2ת�Ƶĵ�����Ϊ4NA��B��ȷ������������ͨ�룬C��ȷ�������ܷ�ӦʽΪN2H4��O2=N2��2H2O�������������ص�Ũ�Ȼή�ͣ�pH��С��D����ȷ����ѡD��
�����Ѷȣ�һ��
4��ѡ���� ijͬѧ��װ����ͼ��ʾ�ĵ绯ѧװ�õ缫IΪAl�������缫��ΪCu����

A���������缫IV��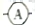 ���缫I ���缫I
B���缫I������ԭ��Ӧ
C���缫II���ܽ�
D���缫III�ĵ缫��Ӧ��Cu2++2e-==Cu
�ο��𰸣�A
���������A���������֪����װ�õ�I��II��ԭ��ص�������I�Ǹ�����II��������III��IV�ǵ��ص�����������III��������IV�����������Ե������缫IV�� ���缫I����ȷ��B���缫I��ԭ��صĸ���������������Ӧ������C���缫II��ԭ��ص�������������ԭ��Ӧ����Cu����������D���缫III������������������Ӧ���缫��Ӧ��Cu-2e-=��Cu2+������ѡA�� ���缫I����ȷ��B���缫I��ԭ��صĸ���������������Ӧ������C���缫II��ԭ��ص�������������ԭ��Ӧ����Cu����������D���缫III������������������Ӧ���缫��Ӧ��Cu-2e-=��Cu2+������ѡA��
�����Ѷȣ�һ��
5��ѡ���� п��ͭ��ϡ������ɵ�ԭ��أ������й�˵����ȷ���ǣ�?��
��п�������ݲ���?�ڵ�����Zn�����·����Cu
�۸�����Zn +2e-=Zn2+?��Cu2+����Һ����Cu����Zn��Ǩ��
A���٢ڢ�
B���ڢ�
C����
D���ڢ�
�ο��𰸣�C
�����������п���Ǹ����������ܽ⣬ͭ�����������������ݣ��ʴ����۸���ʧȥ���ӣ�����������Ӧ���ʴ�����������������������ͭ�����ʴ�����ѡC��
���������⿼��ѧ��ԭ��صĹ���ԭ�������Ը�����ѧ֪ʶ���лش���Ŀ�ѶȲ���
�����Ѷȣ���
| 