1��ѡ���� ijԭ����ܷ�Ӧ���ӷ���ʽΪ2Fe3++Fe=3Fe2+����ʵ�ָ÷�Ӧ��ԭ����ǣ�������
A������Ϊͭ������Ϊ�����������ҺΪFeCl3��Һ
B������Ϊͭ������Ϊ�����������ҺΪFe��NO3��2��Һ
C������Ϊ��������Ϊп���������ҺΪFe2��SO4��3
D������Ϊ��������Ϊ�����������ҺΪCuSO4
�ο��𰸣�A�����Ļ����Դ���ͭ������������ͭ���������������ҺΪ�Ȼ�������������ʵ�ָ÷�Ӧ��ԭ��أ���A��ȷ��
B�����Ļ����Դ���ͭ������������ͭ���������������ҺΪ����������������ʵ�ָ÷�Ӧ��ԭ��أ���B��ȷ��
C��п�Ļ����Դ�������п�������������������������ҺΪ�������������Dz���ʵ�ָ÷�Ӧ��ԭ��أ���C����
D�����Ļ����Դ����������������������������������ҺΪ����ͭ�������Dz���ʵ�ָ÷�Ӧ��ԭ��أ���D����
��ѡAB��
���������
�����Ѷȣ�һ��
2������� �г��ϳ��۵ġ��ȷ��������Ҫ�ɷ�����м��̿�ۡ�ľм�������Ȼ��ƺ�ˮ�ȡ����ȷ��������֮ǰ�����ϴ�ʹ�����������������ʱ�������ϴ��������ͻ�ų�������ʹ����ᷢ���д���������ڡ�
��1���ȷ��������________�ų�������
��2��̿�۵���Ҫ������__________________________________��
��3�������Ȼ��Ƶ���Ҫ������____________________________��
��4��ľм��������______________________________________��
��5���йصĵ缫��Ӧʽ�ͻ�ѧ����ʽ��____________________________________________��
�ο��𰸣���1����������
��2������м��NaCl��Һ����ԭ��أ�������м������
��3��NaCl����ˮ���γɵ������Һ
��4��ʹ�á��ȷ����ʱ���Ⱦ���
��5��������Fe��2e��=Fe2����������O2��2H2O��4e��=4OH����Fe2����2OH��=Fe��OH��2����4Fe��OH��2��O2��2H2O=4Fe��OH��3
�������������˿����������ȼ��ͬʱѸ�ٷų��������ȣ�����֪���ڳ�ʪ�����������ʱҲ��ų�������ֻ�DZ�ȼ�ջ���һЩ��
�ճ���������������ڻ������������ͷ�Ҳ�dz����������Ծ��쵽�������ṩ�ʵ������������Ũ�ĵ������Һ�������Ҳ����õĹ������ʣ�������Ϊԭ��صĸ������ϣ������������ʾͻ���ӿ졣ľм���������á��ȷ�����������������ȵ�����ɢʧ�����ݡ���м��̿�ۼ�NaCl��Һ����ԭ��أ�����������̿��������������ѧ��ת��Ϊ���ܣ��ų�������
�����Ѷȣ�һ��
3��ѡ���� ��ͼ��ʾ��������ָ�뷢��ƫת��X����֣�Y����ϸ��������������������(? )
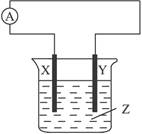
A��X��Cu,Y��Zn��Z��ϡH2SO4��Һ
B��X��Zn��Y��C��Z��CuSO4��Һ
C��X��Fe,Y��Cu,Z��Fe(NO3)3��Һ
D��X��Ag��Y��Zn,Z��AgNO3��Һ
�ο��𰸣�D
����������������֪X���Ǹ�ԭ��ص�������Y���Ǹ�����ֻ��Dѡ��������⡣
�����Ѷȣ���
4��ѡ���� ����������ȷ����?
[? ]
A������п�̵�صĸ�������Ϊ��������
B����������ȼ�ϵ�ع���ʱ������ӦΪ��H2+2OH-- 2e - =2H2O
C��Ǧ���طŵ�ʱ������ӦΪ��PbO2+4H++ 2e-= Pb2+ +2H2O
D��п-ͭ-ϡ���ṹ�ɵ�ԭ��ع���ʱ��H+���ƶ�
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5������� �ס������ص缫���϶���������̼��������ͼ������ش��������⣺?
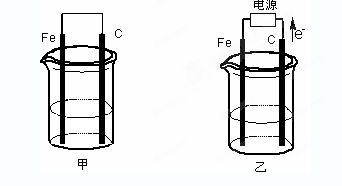
(1)�������о�ʢ��CuSO4��Һ����Ӧһ��ʱ���
���к�ɫ�����������ǣ��׳��е�?�����ҳ��е�?����
�����ҳ��������ĵ缫��Ӧʽ��?��
(2)�������о�ʢ�ű���NaCl��Һ��
��д���ҳ��з����ܷ�Ӧ�����ӷ���ʽ?��
�ڽ�ʪ��ĵ���KI��ֽ�����ҳظ�����������ֽ��������һ��ʱ����ַ�����ɫ��ȥ��������Ϊ������Cl2�����ɵ�I2����������Ӧ��Cl2��I2�����ʵ���֮��Ϊ5:1�������������ᡣ�÷�Ӧ�Ļ�ѧ����ʽΪ ?��
�����ҳ�ת��0.02mol���Ӻ�ֹͣʵ�飬������Һ�������200mL������Һ���Ⱥ��pH= ?��
�ο��𰸣�(1)�� ̼(C )����(Fe) (2��)?�� 4OH�D�D4e����2H2O + O2��? (2��)
(2)��2Cl��+2H2O 2OH��+H2��+Cl2��(2��)?��5Cl2 + I2 + 6H2O��10HCl + 2HIO3 (2��)?��13 (2��)
2OH��+H2��+Cl2��(2��)?��5Cl2 + I2 + 6H2O��10HCl + 2HIO3 (2��)?��13 (2��)
�����������1���ٸ���װ��ͼ��֪���׳�Ϊԭ��أ�ԭ����л��ý���������������������Ӧ��̼������������Cu�������ҳ�Ϊ���أ����·���������Դ����������̼��Ϊ�������ų��������������缫�Ϸ�����ԭ��Ӧ��Cu������
���ҳ��У����Ե缫Ϊ�������������ͭ��Һ���������������ӷŵ������������缫��ӦΪ4OH�D�D4e����2H2O + O2����
��2�������������ҺΪ�����Ȼ�����Һ�����ҳؾ����ö��Ե缫Ϊ��������Ȼ�����Һ���ܵ����ӷ�Ӧ����ʽΪ2Cl��+2H2O 2OH��+H2��+Cl2����
2OH��+H2��+Cl2����
�ڷ�Ӧ��Cl2��I2�����ʵ���֮��Ϊ5:1�������������ᣬ����һ�������ᡣ���ݵ��ӵĵ�ʧ�غ��֪��Ԫ�صĻ��ϼ�Ӧ�����ߵ���5�ۣ��������������ǵ��ᣬ��˷�Ӧ�ķ���ʽ��5Cl2 + I2 + 6H2O��10HCl + 2HIO3��
�۵���Ȼ�����Һ�ķ���ʽΪ2Cl��+2H2O 2OH��+H2��+Cl2�����ҳ�ת��0.02mole-������0.02mol���������ƣ���������NaOH��Һ�����ʵ���Ũ��c��0.02mol��0.2L��0.1mol/L����pH��13��
2OH��+H2��+Cl2�����ҳ�ת��0.02mole-������0.02mol���������ƣ���������NaOH��Һ�����ʵ���Ũ��c��0.02mol��0.2L��0.1mol/L����pH��13��
�������������е��Ѷȵ����⣬Ҳ�Ǹ߿��еij������͡������������У���ע�ض�ѧ������֪ʶ���̺�ѵ����ͬʱ�����ض�ѧ������������������ʱҪ��ȷ��ͬװ�����������ĵ缫��Ӧ����Ϥԭ��غ͵��صĹ���ԭ�����ɽ��
�����Ѷȣ�һ��