1、选择题 能正确表示下列反应的离子方程式是
A.少量Cl2通入KI溶液中:Cl2+ 2I- =2C1- + I2
B.碳酸钙溶于稀硝酸中:CO2- 3 + 2H+ =H2O + CO2↑
C.醋酸钠水溶液中通入足量CO2:2CH3COO- + CO2 + H2O = 2CH3COOH + CO2- 3
D.金属铝溶于稀硫酸中:Al + 2H+ = A13+ + H2↑
参考答案:A
本题解析:碳酸钙难溶于水,应该用化学式表示,B不正确;C中CO2是足量的,生成物应该是碳酸氢钠,C不正确;D中电子的得失不守恒,应该是2Al + 6H+=2A13+ + 3H2↑,答案选A。
点评:该题是高考中的常见题型,所以侧重对学生能力的考查,属于中等难度的试题。判断离子方程式正确与否的方法一般是:(1)检查反应能否发生。(2)检查反应物、生成物是否正确。(3)检查各物质拆分是否正确。(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等)。(5)检查是否符合原化学方程式。
本题难度:简单
2、选择题 下列离子方程式中正确的是:
A.少量SO2通入NaOH溶液中:OH-+SO2→HSO3-
B.H2S通入氯水中:S2-+Cl2 →S↓+2Cl-
C.二氧化氮溶于水:3NO2+H2O →2H++2NO3-+NO↑
D.少量NaHSO4与过量Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH- →BaSO4↓+2H2O
参考答案:C
本题解析:A.碱过量,产物应该为正盐,错误
B.H2S酸为弱电解质,不能拆,不正确
C.正确
D.NaHSO4不足,则H+与SO42-系数保证为1,不正确
答案为C
本题难度:一般
3、选择题 下列反应的离子方程式书写正确的是(?)
A.钠和冷水反应:Na+2H2O Na++2OH-+H2↑
Na++2OH-+H2↑
B.金属铝溶于氢氧化钠溶液:Al+2OH- AlO2-+H2↑
AlO2-+H2↑
C.金属铝溶于盐酸中:2Al+6H+ 2Al3++3H2↑
2Al3++3H2↑
D.铁跟稀硫酸反应:Fe+2H+ Fe2++H2↑
Fe2++H2↑
参考答案:CD
本题解析:A中得失电子和电荷均不守恒,对应的离子方程式为2Na+2H2O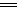 2Na++2OH-+H2↑;B项中电荷和得失电子均不守恒,对应的反应的离子方程式为2Al+2OH-+2H2O
2Na++2OH-+H2↑;B项中电荷和得失电子均不守恒,对应的反应的离子方程式为2Al+2OH-+2H2O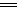 2AlO
2AlO +3H2↑。
+3H2↑。
本题难度:简单
4、选择题 能正确表示下列反应的离子方程式是 (?)
A.用过量氨水吸收工业尾气中的SO2:2NH3・H2O+SO2=2NH4++SO32-+H2O
B.氯化钠与浓硫酸混合加热:H2SO4+2Cl- SO2↑+Cl2↑+H2O
SO2↑+Cl2↑+H2O
C.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+3H2O
D.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-=2BaSO4↓+Al(OH)3↓
参考答案:A
本题解析:以学过的元素化合物知识和离子反应的书写原则逐项分析。
A项过量氨水与SO2反应生成(NH4)2SO3;B项氯化钠与浓硫酸反应的生成物应为HCl、NaHSO4或HCl、Na2SO4;C项磁性氧化铁Fe3O4不能写成离子形式;D项要使SO42-恰好完全沉淀,KAl(SO4)2・12H2O与Ba(OH)2的物质的量之比应为1∶2,此时应该生成AlO2-。
本题难度:一般
5、选择题 下列实验设计及其对应的离子方程式均正确的是
[? ]
A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+ =Cu2+ + 2Fe2+
B.Na2O2与H2O反应制备O2:Na2O2 + H2O =2Na+ + 2OH- + O2↑
C.将氯气溶于水制备次氯酸:Cl2 + H2O =2H+ + Cl- + ClO-
D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO4- +6H+ + 5H2O2 =2Mn2+ + 5O2↑ + 8H2O
参考答案:A
本题解析:
本题难度:一般