|
高中化学必备知识点《难溶电解质的溶解平衡》答题技巧(2019年最新版)(六)
2019-06-28 21:26:59
【 大 中 小】
|
1、选择题 常温下,取一定量的PbI2固体配成饱和溶液 ,T时刻改变某一条件,离子的浓度变化如图所示,(注:第一次平衡时c(I-)=2x10-3mol/L, c(Pb2+)=1x10-3mol/L)下列有关说法正确的是

A.常温下,Ksp=2x10-6
B.温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,PbI2的溶解度不变,c(Pb2+)不变
C.T时刻改变的条件是升高温度,PbI2的,Ksp 增大
D.常温下Ksp[PbS]=8x10-28,向PbI2的悬浊液中加入Na2S溶液,PbI2(s)+S2-(aq) PbS(s)+2I-(aq)反应的化学平衡常数为5x1018 PbS(s)+2I-(aq)反应的化学平衡常数为5x1018
|
参考答案:D
本题解析:A、PbI2(s)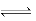 Pb2+(aq)+2I-(aq),Ksp=[c(Pb2+]×[c(I-)]2=1×10-3×4×10-6=4×10-9,错误;B、PbI2(s) Pb2+(aq)+2I-(aq),Ksp=[c(Pb2+]×[c(I-)]2=1×10-3×4×10-6=4×10-9,错误;B、PbI2(s)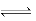 Pb2+(aq)+2I-(aq),加入硝酸铅浓溶液,反应向逆反应方向进行,PbI2的溶解度降低,错误;C、T时刻升高温度,根据图像c(I-)是降低,说明反应向逆反应方向进行,溶解度降低,错误;D、K=c2(I-)/c(S2-)= Pb2+(aq)+2I-(aq),加入硝酸铅浓溶液,反应向逆反应方向进行,PbI2的溶解度降低,错误;C、T时刻升高温度,根据图像c(I-)是降低,说明反应向逆反应方向进行,溶解度降低,错误;D、K=c2(I-)/c(S2-)= 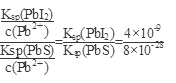 =5×1018A,正确。 =5×1018A,正确。
考点:考查溶度积的计算和勒夏特列原理。
本题难度:一般
2、选择题 在溶液中有浓度均为0.0lmol/L的Fe3+、Cr3+、Zn2+、Mg2+等离子,已知:
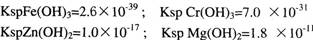
当氢氧化物开始沉淀时,下列哪一种离子所需的pH最小(? )
A.Fe3+
B.Cr3+
C.Zn2+
D.Mg2+
参考答案:A
本题解析:略
本题难度:简单
3、选择题 已知:Ksp(Ag2SO4)=1.4×10-5,Ksp(BaSO4)=1.1×10-10,Ksp(CaSO4)=9.1×10-6,Ksp(BaCO3)=2.6×10-9。则下列说法中不正确的是
[? ]
A.有关的四种盐中溶解性最强的是Ag2SO4
B.有关的三种硫酸盐中,其饱和溶液中硫酸根离子浓度最小的是BaSO4
C.CaSO4沉淀能较容易地转化成为BaSO4沉淀
D.BaSO4沉淀不可能会转化成BaCO3沉淀
参考答案:D
本题解析:
本题难度:一般
4、选择题 下列说法正确的是
A.能使pH试纸呈红色的溶液中可能大量存在以下离子:Na+、NH4+、I一、NO3-
B.将CH3COOH溶液和NaOH溶液等体积混合,该溶液中一定存在的关系式为:c(Na+)=c(CH3COO一)+c(CH3COOH)
C.pH=3的NaHA溶液中粒子浓度大小为:c( Na+)>c( HA一)>c(A2一)>c(H2A)>c(OH一)
D.CuSO4溶液遇到闪锌矿(ZnS)慢慢转化为铜蓝(CuS),是因为ZnS的溶解度大于CuS
参考答案:D
本题解析:A项为酸性溶液,I一和NO3-在酸性条件下发生氧化还原反应,而不能大量共存;B项溶液的浓度未知,所以无法确定关系;C项溶液的浓度未知,不能确定HA-是否水解,错误;D项体现难溶电解质间的转化。
考点:离子共存问题、离子浓度大小的比较、难溶电解质的沉淀溶解平衡。
本题难度:困难
5、选择题 Al(OH)3难溶于水,某温度下,只要溶液中Al3+物质的量浓度(mol/L)和OH-物质的量浓度(mol/L)3次方的乘积大于1.9×10-33,就会析出Al(OH)3沉淀,则0.10mol/L?AlCl3不产生沉淀的最大OH-物质的量浓度(mol/L)为( )
A.1.9×10-33
B.2.7×10-11
C.8.7×10-8
D.1.2×10-11
参考答案:由题意知Ksp[Al(OH)3]=c(Al3+)×c3(OH-)=1.9×10-33,若溶液中不产生沉淀,则有c(Al3+)×c3(OH-)<1.9×10-33,
即0.1×c3(OH-)<1.9×10-33,c(OH-)<31.9×10-330.1
本题解析:
本题难度:一般
|