1、实验题 (12分)温度对化学反应速率影响的实验探究根据下图所给出的仪器和药品进行实验。

操作方法:在三支相同的试管中分别加入2 mL―3 mL约5%的H2O2,然后在每支试管中滴加2滴1 mol・L-1的FeCl3溶液后立即套上气球(大小相同)。等三支试管上的气球大小差不多相同时,同时置于三个烧杯中观察现象。
实验现象为___________________________________________________________________。
实验结论为___________________________________________________________________。
参考答案:气球膨胀的由快到慢的顺序为左→中→右
升高温度加快反应速率,降低温度减慢反应速率
本题解析:H2O2在不同温度下的分解速率不同,很明显,温度越高,反应速率越快,FeCl3在此作催化剂。
本题难度:简单
2、实验题 (10分)实验小组测定某肥料中的总氮含量(以氮的质量分数表示) ,实验装置如下图(图中加热及夹持仪器略去):
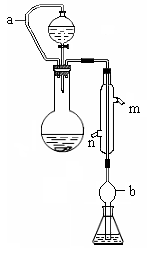
称取1.200 g样品,通过化学方法将肥料中的氮转化成铵盐(除样品外,所加试剂均不含氮元素),然后在碱性溶液中蒸馏氨,用25.00 mL浓度为0.5000 mol/L-1硫酸溶液充分吸收,再用浓度为0.1000 mol/L-1氢氧化钠溶液滴定未反应的硫酸。重复上述实验三次。实验数据如下:
实验次数
| 氢氧化钠溶液的体积
|
滴定前刻度(mL)
| 滴定后刻度(mL)
|
1
| 0.00
| 5. 01
|
2
| 6.00
| 10.99
|
3
| 12.00
| 17.60
|
?
(1)写出圆底烧瓶内发生反应的离子方程式?。
(2)分液漏斗和圆底烧瓶之间的导管a的作用是?;? b的作用是?
?;冷凝管中从(填“n”或“m”)?口进水。
(3)在滴定过程中,以下操作会使所测总氮含量偏小的是(填序号) ? ?。
A.锥形瓶水洗后未烘干
B.滴定过程中滴定管有漏水现象
C.滴定过程中有少量溶液从锥形瓶中溅出
D.滴定前滴定管内有气泡,滴定后没有了