1������� Ϊ���Ƶ�������̽��������һЩ��ѧ���ʣ�ijѧ������ͼ��ʾװ�ý����й�ʵ�飬��A�IJ���������A��Ũ������Һ��μ���װ�ж������̵�B�С��Իش�
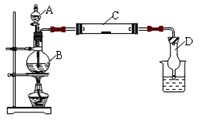
��1����������װ�õ�������??��
��2����C��Ϊ����KI��ֽ��ʵ��Ƭ�̺�C�п��Թ۲쵽��ʵ������Ϊ?��д��
B�з�����Ӧ�����ӷ���ʽ?��
��3����C�еĵ���KI��ֽʵ��һ��ʱ����ֱ�Ϊ��ɫ��ԭ����?��
��4��D��������_______________���ձ��м������??��
��5����ʵ������ʱ�������̣����ô�װ����ȡ������ѡ��?ҩƷ�������ʵ������ʱ��Ũ���ᣬ���ô�װ����ȡ������ѡ��?ҩƷ�����
�ο��𰸣���12�֣���1���رշ�Һ©��������ƿ�����ȣ����ձ����Ƿ������ݲ�������ȴ��D���Ƿ����ˮ������2�֣�
��2����ֽ����ɫ��1�֣���MnO2 +2Cl- +4H+ ? ?Mn2+? +Cl2�� +2H2O��2�֣�
?Mn2+? +Cl2�� +2H2O��2�֣�
��3����KI������KIO3 (2��)
��4����������1�֣�����������Һ��1�֣�
��5��KMnO4��KClO3(���� ����)��2�֣���NaCl��Ũ���ᣨ1�֣�
����)��2�֣���NaCl��Ũ���ᣨ1�֣�
�����������
�����Ѷȣ�һ��
2��ʵ���� ��20�֣�ʵ����
���������й�SO2��Cl2������ʵ�顣
(1)ijС�������ͼ��ʾ��װ��ͼ��ͼ�мгֺͼ���װ����ȥ�����ֱ��о�SO2��Cl2�����ʡ�
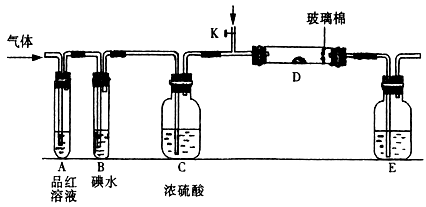
������˷ֱ�ͨ��SO2��Cl2��װ��A�й۲쵽�������Ƿ���ͬ��?(���ͬ������ͬ��)����װ��D��װ����V2O5(����)��ͨ��SO2ʱ����Kͨ������O2�Ļ�ѧ��Ӧ����ʽΪ?��
��SO2ͨ��B�У���Һ��ɫ��ȥ����÷�Ӧ�����ӷ���ʽΪ?��
(2) ijͬѧ��������SO2ͨ��һ֧װ���Ȼ�����Һ���Թܣ�δ���������ɣ�������Թ��м�������(����ĸ)?����Ȼ���۲쵽����������
A����ˮ? B��ϡ����? C���������Һ? D��������Һ
(3)����Ԫ��S��O��ɨC2���������X��X��S��O��������Ϊ2��3����Cl2�뺬X����Һ��ȫ��Ӧ�ó�����Һ��ȡ��������Һ���������ữ���Ȼ�����Һ���а�ɫ����������д��Cl2�뺬X����Һ��Ӧ�����ӷ���ʽ?��?
(4)ij���е�λ���õ绯ѧԭ����SO2���Ʊ����ᣬװ����ͼ
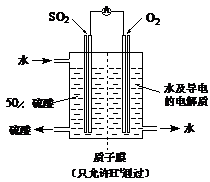
����ij�ִ������缫Ϊ��IJ��ϣ����������壬ͬʱҲ��ʹ������������Һ��ֽӴ���ͨ��SO2�ĵ缫Ϊ_________������缫��ӦʽΪ?����ص��ܷ�Ӧʽ?
��ʵ���ǻ�ѧ�о��Ļ������������и�װ��ͼ��������ȷ����?������ţ�
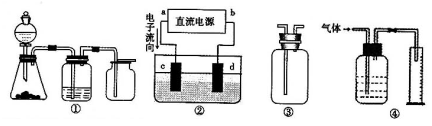
A��װ�âٿ���ɶ�������ķ������������ռ�����ͭм��ϡ���ᷴӦ
B��װ�â��У�aΪ������dΪ����
C��װ�âۿ������ռ�H2��NH3��Cl2,��HCl��NO2��
D��װ�â������ڲ����������
��?��Ǧ���ص���±ˮ����Cl����Br����Na+��Mg2+����װ����ͼ��ʾ��a��bΪʯī�缫��������˵������ȷ����?������ţ�
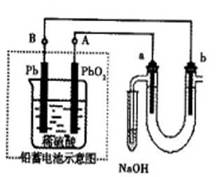
A��Ǧ���ظ����ķ�ӦʽΪ��Pb��2e��=Pb2+
B��Ǧ���طŵ�ʱ��B���������ᣬA����������
C��Ǧ���س��ʱ��A��Ӧ�����Դ��������
D������±ˮʱ��a�缫���ȷŵ����Br��
�ο��𰸣��� (1) ����ͬ? 2SO2 + O2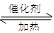 2SO3
2SO3
��SO2 + I2 + 2H2O = 4H��+ 2I��+ SO42��?
(2) B
(3) Cl2 + SO32��+H2O = SO42��+ 2Cl��+ 2H��
(4) ��? SO2 �C 2e��+ 2H2O = 4H��+ SO42��? 2SO2 + O2 + 2H2O = 2H2SO4
�� C
��? D
�����������1��������SO2��Cl2������ʹƷ����Һ��ɫ������A�зֱ�ͨ��SO2��Cl2���۲쵽����������ͬ�ġ�
��װ��D��װ��������������(����)��ͨ��SO2ʱ����Kͨ������O2������SO2�Ĵ���������Ӧ����ʽΪ2SO2 + O2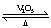 2SO3��
2SO3��
��SO2ͨ��B�У���ˮ��ɫ��������SO2��Ư�����ã�����SO2��ԭ��Ϊ��ɫ�����ʣ����ӷ���ʽΪ��SO2 + I2 + 2H2O = 4H��+ 2I��+ SO42��
��2��SO2ͨ��װ���Ȼ�����Һ����ֻ��ˮ���������ᣬ�õ�������Һ�������Ȼ����Dz�������ѧ��Ӧ�ģ��������ǿ�ᣩ���������ɣ�
A�����백ˮ���ɵõ�SO3�����������ɳ�����SO3��+Ba2+=BaSO3��
B������ϡ���ᣬ��Ӧ��������������
C������������£�NO3������ǿ�����ԣ��ɽ�SO3������ΪSO42���������õ�BaSO4����
D������������£�+4�����롪2���������з�Ӧ������dz��ɫ������
��3����S��O��������Ϊ2��3��֪����Ԫ�صĸ�����Ϊ1:3����XΪSO32���������ӱ���������SO42�������ӷ���ʽΪ��Cl2 + SO32��+H2O = SO42��+ 2Cl��+ 2H��
��4����װ��Ϊԭ��أ�ԭ��ص�����������ԭ��Ӧ����������������Ӧ�����������õ���Ϊ������O2��4e����4H��=2H2O���ܷ�ӦΪ��2SO2 + O2 + 2H2O = 2H2SO4��
���ܷ�Ӧ��ȥ������Ӧ�ɵø����缫��ӦΪ��SO2 �C 2e��+ 2H2O = 4H��+ SO42��
��A��ͭм��ϡ�����ڼ��������²ſɷ�Ӧ������ȷ
B��a���������ӣ�Ϊ����������ȷ
C������������������Ӧ��ͨ���ı�����ڷֱ�������ϻ��������������ռ�����ȷ
D�����ڽ������ܳ������������̣ܶ��ʲ����ų�Һ�壬����ȷ
��A��Ǧ���ظ����ķ�ӦʽΪ��Pb��2e��+SO42��=PbSO4
B��Ǧ���طŵ�ʱ��Pb��PbO2��ת��ΪPbSO4���������������ӣ�����ȷ
C��Ǧ����A��Ϊ������������ʱӦ�����Դ��������
D��a��Ϊ�����������ӷŵ磬���ݷŵ�˳���֪�����ȷŵ����Br������ȷ
��ѡD
�����Ѷȣ���
3������� �����£���һ��Ũ�ȵ�Na2CO3��Һ����CnSO4��Һ�еõ�����ɫ������Ϊ��ȷ����������ɣ�ij�о���ѧϰС�����������������о���
(һ���������˵��
����һ�����߷�Ӧֻ����CuCO3���ֳ�����
���������������ٽ�ˮ�⣬����Cu(OH)2���ֳ�������˷�Ӧ��ѧ����ʽΪ��____________________________��
�����������ɵ���CuCO3��Cu(OH)2���ֳ�����
(����������̽����
�������ϣ�CuCO3�� Cu(OH)2�������ᾧˮ��
Cu(OH)2�������ᾧˮ��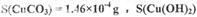
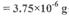 �����ɴ������жϣ�����_______�Dz���ȷ�ġ�
�����ɴ������жϣ�����_______�Dz���ȷ�ġ�
(����[ʵ��̽��]
����һ����CuCO4��Һ�����Ũ�ȵ������Na2CO3��Һ�в����裬����ɫ�������ɡ�
�����������������Һ�з�����������������Ϊ���ٹ��ˣ���_______,�۸��
��������������ͼ��ʾװ�ã����ж���������
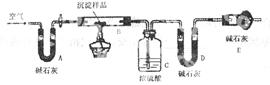
��������װ�ú�����Ҫ���е�ʵ�������_____________________��
��ʵ�����ʱͨ�����������������_____________________��
�����ݼ�¼�ͷ�����ʵ������вⶨ�������У�W1������Ʒ��������W2������Ӧ��װ��B�в�����������W3������Ӧ���ɵ�ˮ��������W4������Ӧ�����ɶ�����̼��������Ϊ�˲ⶨ����ɣ�������Ҫ����? �����ݣ��뽫���ܵ���������±��У�ÿ���ո�����һ����ϣ��м�����Ͼ���֣���������.��
�ο��𰸣���һ���������Na2CO3 +CuSO4 +H2O=Cu��OH��2��+Na2SO4+CO2����3�֣�
������һ ��2�֣�
������ �������ϴ�ӣ�1�֣�
���������ټ��װ�õ������� ��2�֣�
�ڱ�֤װ���е�ˮ������CO2��C��Dװ����ȫ���գ�2�֡�ֻҪ��������������2�֣�
��2��2�֣�
W1W2
W1W3
W1W4
W2W3
W2W4
W3W4
?
?
��ÿ���2���1�֣�������0.5�֣���3�֣�
�����������
�����Ѷȣ�һ��
4��ʵ���� ��10�֣�ij̽����ѧϰС������С����״����Ͻ�������ϡ����ķ�Ӧ�����й���ϡ�����Ӧ���ⶨͨ��״����Լ20�棬1 atm��������Ħ������ķ�������ѡ������ʵ��װ��������飺
��1������ͬѧ����ѡ�õ�װ�õ�����˳���ǣ��ùܿ���ĸ���ɲ���������
A�ӣ�?����?���ӣ�?����?���ӣ�?��
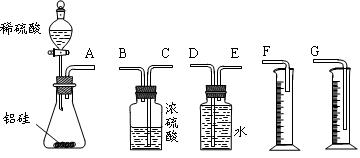
��2��ʵ�鿪ʼʱ���ȴ�Һ©���ϿڵIJ���������������������һ�����ϡ����Ҳ����˳��������ƿ�������������ԭ��_________________________��
��3��ʵ�����ʱ������ͬѧӦ��������ʵ�������������������_______________��
��4��ʵ����ȷ���4�����ݣ�ʵ��ǰ����Ͻ������m1 g��ʵ���������������m2 g��ʵ�����Ͳ��Һ�����ΪVmL����ͨ��״��������Ħ�����Vm��_________�����Ͻ��к�ͭ����õ�Vm��________��ƫ��/ƫС/��Ӱ�죩��
�ο��𰸣���1��E D G?
��2������ϡ���ᷴӦ�������������壬ʹ��ƿ������ѹǿ���?
��3����ʵ��װ����ȴ�������ƶ���Ͳʹ����Һ������ƿ��Һ����ƽ����ƽ�Ӷ�ȡ��Ͳ��ˮ���������������ͨ��״��ʱ������������������1�֣�
��4��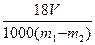 ?L��moL��1?��Ӱ��
?L��moL��1?��Ӱ��
�����������
�����Ѷȣ�һ��
5������� Ϊ����֤þ�����Ľ�����ǿ����ijͬѧ�����ʵ����֤���ṩ���Լ��У�þ����������ˮ�����ᡢŨ���ᣮ
��1����ѡ�Լ�Ϊ______��
��2��������Ӧ�Ļ�ѧ����ʽΪ______��
��3�����Ҫ������������̼�����______��
�ο��𰸣���1������þ���������ᷴӦ�������������ʲ�һ��������֤�������Ļ�����ǿ�����������ڳ���������Ũ���ᷢ���ۻ���������Ũ���ᣬ�ʴ�Ϊ��þ�������������
��2������þ���������ᷴӦ�ֱ�Ϊ��Mg+2HCl�TMgCl2+H2����2Al+6HCl�T2AlCl3+3H2�����ʴ�Ϊ��Mg+2HCl�TMgCl2+H2����2Al+6HCl�T2AlCl3+3H2����
��3����þ���������ֱ����ʢ��Ũ����ȵ�������Һ�У��۲�������������ʣ��������������ʿ���ǽ���þ����֮�ǽ��������ʴ�Ϊ����þ���������ֱ����ʢ��Ũ����ȵ�������Һ�У��۲�������������ʣ��������������ʿ���ǽ���þ����֮�ǽ�������
���������
�����Ѷȣ�һ��