1、选择题 下列有关工业生产叙述正确的是( )
A.工业上通常使用电解法制备金属钠、镁、铝等
B.合成氨工业中,将NH3及时液化分离有利于加快反应速率
C.硫酸工业中,采用常压条件的原因是此条件下催化剂活性最高
D.电解精炼铜时,将粗铜与电源的负极相连
参考答案:A、活泼金属冶炼是利用电解熔融的金属氯化物得到,故A正确;
B、合成氨工业中,将NH3及时液化分离,浓度减小,速率减小,故B错误;
C、常采用常压条件的原因是,压条件二氧化硫的转化率易很大,加压转化率增大不大,故C错误;
D、电解精炼铜时,将粗铜与电源的正极相连,做电解池的阳极,失电子发生氧化反应,故D错误;
故选A.
本题解析:
本题难度:简单
2、选择题 在2L恒容密闭容器中充入2 mol X和1mol Y发生反应:2X(g)+Y(g) 3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
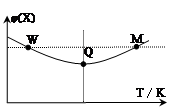
A.升高温度,平衡常数增大
B.W点X的正反应速率等于M点X的正反应速率
C.Q点时,Y的转化率最大
D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大
参考答案:C
本题解析:A、分析图像,X的体积分数先减小后增大,减小到最低,这是化学平衡的建立过程,后增大,这是平衡的移动过程,升高温度,体积分数增大,说明升高温度,平衡向左移动,使平衡常数减小,故A错误; B、M点温度高,故反应速率快,B错误;从开始到Q点是正向建立平衡的过程,转化率逐渐增大,从Q到M点升高温度,平衡向左移动,使转化率降低,Q点最大,故C正确;平衡时再充入Z,达到的新平衡与原平衡是等效平衡,体积分数相等,故D错误;故选C。
本题难度:一般
3、选择题 下列各组反应(表内物质均为反应物)刚开始时,放出H2速率最大的是
编号
| 金属(粉末状)
| 物质的量
| 酸的浓度
| 酸的体积
| 反应温度
|
A
| Al
| 0.1 mol
| 18.4 mol/L H2SO4
| 10 mL
| 60 ℃
|
B
| Mg
| 0.1 mol
| 3 mol/L HCl
| 10 mL
| 30 ℃
|
C
| Fe
| 0.1 mol
| 3 mol/L H2SO4
| 10 mL
| 60 ℃
|
D
| Mg
| 0.1 mol
| 3 mol/L H2SO4
| 10 mL
| 60 ℃
|
参考答案:D
本题解析:根据金属活动性,Mg的活泼性最强;浓硫酸水太少,很难电离,所以H+浓度最大的溶液为3mol?L?1 H2SO4,;温度越高,反应速率越大,所以放出H2速率最大的是D项。
考点:本题考查化学反应速率的比较。
本题难度:一般
4、选择题 在气体反应中,能使反应物中活化分子数和活化分子百分数同时增大的方法是( )
①增大反应物的浓度 ②升高温度 ③移去生成物 ④增大压强 ⑤加入催化剂.
A.①③
B.②④
C.②⑤
D.①⑤
参考答案:增大反应物的浓度和增大压强,只能增大活化分子数,不能增大活化分子百分数,而②和⑤既能增大活化分子数,又能增大活化分子百分数,移去生成物,浓度降低,活化分子和活化分子的百分数都减小,
故选C.
本题解析:
本题难度:简单
5、选择题 用足量铁片与稀硫酸反应制取氢气时,下列措施能使氢气生成速率变快但不影响氢气量的是
[? ]
A.加少量Na2SO4固体
B.加少量CuSO4晶体
C.不用稀硫酸,改用98%浓硫酸
D.不用铁片,改用铁粉
参考答案:BD
本题解析:
本题难度:一般