1、选择题 在N2+3H2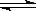 2NH3反应中,自反应开始至2S末,氮气的浓度由0变为0.4mol/L,则以氮气的浓度变化表示该反应在2S内的平均反应速率是( )
2NH3反应中,自反应开始至2S末,氮气的浓度由0变为0.4mol/L,则以氮气的浓度变化表示该反应在2S内的平均反应速率是( )
A.0.2mol/L・S
B.0.4mol/L・S
C.0.6mol/L・S
D.0.8mol/L・S
参考答案:A
本题解析:根据N2+3H2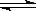 2NH3,自反应开始至2S末,氮气的浓度由0变为0.4mol/L,所以v(N2)=0.4/2=0.2mol/L・S?,故本题的答案选择A。
2NH3,自反应开始至2S末,氮气的浓度由0变为0.4mol/L,所以v(N2)=0.4/2=0.2mol/L・S?,故本题的答案选择A。
点评:本题考查化学反应速率的计算,属于对基础知识的考查,本题比较简单。
本题难度:一般
2、选择题 下列措施对增大反应速率明显有效的是
[? ]
A.Na与水反应时增大水的用量
B.Fe与稀硫酸反应制取氢气时,改用浓硫酸
C.在K2SO4与BaCl2两溶液反应时,增大压强
D.将铝片改为铝粉,做铝与氧气反应的实验
参考答案:D
本题解析:
本题难度:一般
3、选择题 在日常生活中,与化学反应速率有关的做法是
[? ]
A.用热水溶解蔗糖以加速溶解
B.把块状煤碾成粉状再燃烧
C.真空包装食品以延长保质期
D.低温冷藏使食品延缓变质
参考答案:ABD
本题解析:
本题难度:简单
4、选择题 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是 (? )

A.反应开始到10s,用Z表示的反应速率为0.158mol/(L・s)
B.反应开始到10s, X的物质的量浓度减少了0.79mol/L
C.反应开始时10s, Y的转化率为79.0%
D.反应的化学方程式为:X(g)+ Y(g) Z(g)
Z(g)
参考答案:C
本题解析:A.根据题给图像知,10s内Z的物质的量变化量为1.58mol,根据v=△n/V△t计算10s内,用Z表示的反应速率为v(Z)=0.079moL/(L?s),错误;B、根据题给图像知,反应开始到10s, X的物质的量减少了0.79mol,,错误; C、根据题给图像知,反应开始时10s, Y的转化率为79.0%,正确; D、根据题给图像知,随反应进行X、Y的物质的量逐渐减小,Z的物质的量逐渐增大,则X、Y是反应物,Z是生产物,l0s后X、Y、Z的物质的量不变,则反应是可逆反应,且△n(X):△n(Y):△n(Z)=(1.20-0.41)mol:(1.00-0.21)mol:1.58mol=1:1:2,参加反应的物质的物质的量之比等于化学计量数之比,反应化学方程式为X(g)+Y(g) 2Z(g),错误。
2Z(g),错误。
本题难度:一般
5、选择题 下列说法错误的是
A.在C(s) +H2O(g) 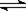 CO(g) + H2(g)反应体系中,增加碳的量不能迅速提高正反应速率
CO(g) + H2(g)反应体系中,增加碳的量不能迅速提高正反应速率
B.钾的金属性比钠强,所以钾与水的反应比钠的反应剧烈
C.在压强相同条件下,结构相似的CH4、SiH4、GeH4的沸点依次升高,所以结构相似的HF、HCl、HBr、HI的沸点也依次升高
D.面粉厂严禁烟火的原因是面粉粉尘表面积大,与空气接触遇明火极易发生爆炸
参考答案:C
本题解析:略
本题难度:简单