1��ѡ���� ���л�ѧ�����ģ����ȷ����
A���Ȼ���ĵ���ʽ��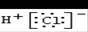

B��N2�ĵ���ʽ��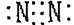
C�������ӽṹʾ��ͼ��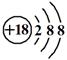
D��������ĵ���ʽ��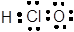
�ο��𰸣�B
����������Ȼ����ǹ��ۻ��������ʽ��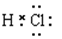 ��A����ȷ�������ӵ���������16����C����ȷ��D����ȷ��Ӧ����
��A����ȷ�������ӵ���������16����C����ȷ��D����ȷ��Ӧ���� �����Դ�ѡB��
�����Դ�ѡB��
�������������е��Ѷȵ����⣬Ҳ�Ǹ߿��еij�����������Ҫ�Ŀ��㡣���������ǿ���������У���Ҫ�ǿ���ѧ���Գ�����ѧ�������Ϥ���ճ̶ȡ�����������Ҫ��ȷ���dz����Ļ�ѧ������Ҫ����Ԫ�ط��š���ѧʽ�����ϼۡ�����ʽ��ԭ�ӽṹʾ��ͼ���ṹʽ���ṹ��ʽ�Լ�����ʽ����ģ�͵ȣ���Ҫ������ס��
�����Ѷȣ���
2��ѡ���� ѧϰ��ѧʱ�������ܶࡰ��ȡ��������йء���ȡ���˵���д�����ǣ�?��
A��ԭ���к����������ͺ��������һ�����
B����Һϡ��ǰ�����ʵ�����һ�����
C���кͷ�Ӧ�вμӷ�Ӧ����ͼ�����һ�����
D�����ʷ�����ѧ�仯ǰ��Ԫ�ص�����һ�����
�ο��𰸣�C
����������кͷ�Ӧ�вμӷ�Ӧ����ͼ�������һ����ȣ�����1mol�����1mol��������ǡ���кͣ��������������36.5g�����������Ƶ�������40g��ѡ��C����ȷ������ѡ�����ȷ�ģ���ѡC��
�����Ѷȣ�һ��
3������� ��200mL?0.5mol/L��ϡ������Һ�м���0.54�����ۣ��ų�448mL����״����NO���壬����ַ�Ӧ����������Һ�м���0.5mol/LNaOH��Һ������0.78���������������������Һ�������
�ο��𰸣�����ϡ������Һ�����۵ķ�Ӧ��Al+4HNO3�TAl��NO3��3+NO��+2H2O���ɷ�Ӧ����ʽ��֪���ų�448mL����״������0.02molNO����ʱ��0.54��Al��0.02mol��ȫ��Ӧ��
HNO3ʣ��0.02mol����������Һ�м���0.5mol/LNaOH��Һ������0.78��������Al��OH��3Ϊ0.01mol��
��һ�������NaOH��Һ��ʣ��������ȫ�к��Ժ���0.01mol��Al3+�γɳ�����
����ҪNaOH��0.02mol���к�ʣ�����ᣩ+0.03mol���γ�0.01molAl��OH��3��=0.05mol��V=0.05mol0.5mol/L=0.1L������Ҫ100ml��
�ڶ��������NaOH��Һ��ʣ��������ȫ�к��Ժ���ȫ����0.02molAl3+�γɳ���������Ӧ�ܽ��0.01mol��Al��OH��3��Al3++3OH-=Al��OH��3����Al��OH��3+OH-=AlO2-+2H2O��
����ҪNaOH��0.02mol���к�ʣ�����ᣩ+0.06mol���γ�0.02molAl��OH��3��+0.01mol���к͵�0.01mol��Al��OH��3��=0.09mol��V=0.09mol0.5mol/L=0.18L������Ҫ180ml��
�𣺼�������������Һ�����Ϊ100ml��180ml��
���������
�����Ѷȣ�һ��
4������� ��1����S+2KNO3+3C=K2S+N2+3CO2�ķ�Ӧ��?Ԫ�ر�������?Ԫ�ر���ԭ��
?����������?�ǻ�ԭ����?���������?�ǻ�ԭ���
��2��ij����A��һ�������¼��ȷֽ⣬���ﶼ�����壬�ֽⷽ��ʽΪ��
2A(s)=" B(g)" + 2C(g) + 2D(g)��ȡһ������A���ȣ���ȫ�ֽ⣬ͬ��ͬѹ�²�����ɵĻ�����������������ܶ�Ϊd����A����Է�������Ϊ?��?
��3������A��B��C��D��ƿ��Һ�����Ƿֱ���NaCl(0.1mol?L-1)��HCl(0.1mol?L-1)��NaOH(0.1mol?L-1)�ͷ�̪��Һ��0.1%���е�һ�֡����˲��������Լ����Ϳ�������һһ����������ʵ�鲽�����£�
�ٸ�ȡ��Һ����������ϣ�������ͬ�ֳ����飻
��ȡһ����Һ�����ϵ�����һ���һ��δ֪��Һ����������ͬ�ɼ����A��B������Һ��
����ȡ�Ѽ����A��Һ2mL, ����3��δ֪C��Һ���ټ���D��Һ4mL���������������������ɫ�仯��
�ۺ�����ʵ���֪��A��B��C��D��Һ�ֱ��ǣ�
A?��? B?��? C?��? D?��
�ο��𰸣�
���������
��ȷ������ظ����ʧ������������ʧ���ӣ����ϼ����ߣ����������ǻ�ԭ�����õ��ӣ����ϼ۽��ͣ�����ԭ������������? C?Ԫ�ر�������? S��N?Ԫ�ر���ԭ��
?S��KNO3?����������? C?�ǻ�ԭ����? CO2?���������? K2S��N2?�ǻ�ԭ���
��
�Ǣٸ�ȡ��Һ����������ϣ�������ͬ�ֳ����飻����һ��ΪNaOH�ͷ�̪��һ��ΪHCl��NaCl
?
NaCl
HCl
NaOH
��̪��Һ
NaCl
�D
�D
�D
�D
HCl
�D
�D
�D
�D
NaOH
�D
�D
�D
��ɫ
��̪��Һ
�D
�D
��ɫ
�D
��ȡһ���ɫ���Һ�����ϵ�����һ���һ��δ֪��Һ����ɫ��ȥ����HCl,��һ������NaCl,�ɼ����A��B������Һ��
����ȡ�Ѽ����A��Һ2mL, ����3��δ֪C��Һ���ټ���D��Һ4mL���������������������ɫ�仯��˵��?A��NaCl,B��HCl,C��NaOH��D�Ƿ�̪��Һ��
�����Ѷȣ�һ��
5��ѡ���� ��һ�������£��ֱ��Ը�����ء�����ء��������⣨2H2O2 =2H2O+O2����Ϊԭ����ȡ���������Ƶ���ͬ����������ʱ��������Ӧ��ת�Ƶĵ�����֮��Ϊ
A��2