1、填空题 [化学――选修物质结构与性质](30分)
Ⅰ.(18分)请选出下列各题中符合题意的选项:
(1)下列物质中,属于含有共价键的离子晶体是?
A.CsCl? B.KOH? C.H2O? D.H2
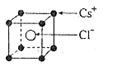
(2)已知CsCl晶体的密度为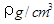 ,NA为阿伏加德罗常数,相邻的两个Cs+的核间距为a cm,如图所示,则CsCl的摩尔质量可以表示为??
,NA为阿伏加德罗常数,相邻的两个Cs+的核间距为a cm,如图所示,则CsCl的摩尔质量可以表示为??
 ?
?
A.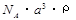 ?g/mol? B.
?g/mol? B.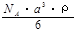 ? g/mol?
? g/mol?
C.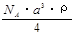 ? g/mol? D.
? g/mol? D.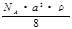 ? g/mol
? g/mol
(3)已知含氧酸可用通式XOm(OH)n来表示,如X是S,m=2,n=2,则这个式子就表示H2SO4。一般而言,该式中m的值越大,该含氧酸的酸性越强。下列各含氧酸中酸性最强的是?
A.HMnO4? B.H2SeO3 ?C.H3BO3? D.H3PO4
Ⅱ.(12分)现有部分前四周期元素的性质或原子结构如下表:
元素编号
| 元素性质或原子结构
|
A
| 原子的电子排布图为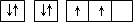
|
B
| 常温下单质为双原子分子,原子间形成三对共用电子对
|
C
| 原子的s轨道电子数等于p轨道电子数,元素的最低负价为-2价
|
D
| 二价阳离子与C的阴离子具有相同的电子层结构
|
E
| 原子序数是D两倍,
|
根据以上情况,回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为?;
(2)B的氢化物的分子空间构型是?;
(3)E在周期表中的位置是?,ECl3能与B、C的氢化物形成配位数为6的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界,ECl3形成的配合物的化学式为?;
(4)AC2在高温高压下所形成的晶胞如右图所示。该晶体的类型属于?(选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中A原子的杂化形式为?;
(5)D 的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:?。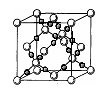
参考答案:Ⅰ.(18分)(1)? B (2)A (3)? A? (每题6分)
Ⅱ.(12分)(1)C<O<N(2分)(2)三角锥形?(2分)
(3)第四周期第ⅥB? [Cr(NH3)4(H2O)2]Cl3(或[Cr(H2O)2 (NH3)4]Cl3)?(4分)
(4)原子?sp3?(2分)
(5)电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量(2分)
本题解析:Ⅰ.(1)A中只有离子键,CD是分子晶体,氢氧化钾中含有离子键和极性键,答案选B。
(2)根据晶胞的结构可知,晶胞含有1个氯离子和1个铯离子,所以有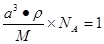 ,所以选项A正确。
,所以选项A正确。
(3)根据通式可知,ABCD分别是MnO3(OH)、SeO(OH)2、B(OH)3、PO (OH)3,因此选项A中酸性最强。所以答案选A
Ⅱ.根据元素性质或原子结构可知,A是碳元素,B是氮元素,C是氧元素,D是镁元素,E是铬元素。
(1)非金属性越强,第一电离能越大,但由于氮元素的2p轨道电子是半充满状态,稳定性强,所以第一电离能大于氧元素的,即C<O<N。
(2)氨气分子中氮原子含有1对孤对电子,所以氨气是三角锥形结构。
(3)铬的原子序数是24,位于第四周期第ⅥB。配位数为6,且氨气和水分子的个数之比是2∶1,所以氨气是4个,水是2个,结构简式为[Cr(NH3)4(H2O)2]Cl3(或[Cr(H2O)2 (NH3)4]Cl3)。
(4)根据晶胞的结构可知,和原子晶体二氧化硅的相似,所以形成的晶体是原子晶体。碳原子与4个氧原子相连,因此是sp3杂化。
(5)镁燃烧时,电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,所以会放出耀眼的白光。
本题难度:一般
2、简答题 【物质结构与性质】
根据元素周期表中第四周期元素的相关知识,回答下列问题:
(1)第四周期元素的基态原子的电子排布中4s轨道上只有1个电子的元素有________种;写出Cu+的核外电子排布式________。
(2)按电子排布,可将周期表里的元素划分成五个区域,第四周期元素中属于s区的元素有________种,属于d区的元素有________种。
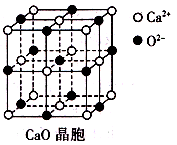
(3)CaO晶胞如所示,CaO晶体中Ca2+的配位数为?;CaO的焰色反应为砖红色,许多金属或它们的化
合物都可以发生焰色反应,其原因是_______。
(4)由叠氮化钾(KN3)热分解可得纯N2:2KN3(s)=2K(l)+3N2(g),下列有关说法正确的是_______(填选项字母)。
A NaN3与KN3结构类似,前者晶格能较小
B晶体钾的晶胞结构如图所示: ,每个晶胞中分摊2个钾原子
,每个晶胞中分摊2个钾原子
C氮的第一电离能大于氧
D氮气常温下很稳定,是因为氮的电负性小
(5)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂。O2在其催化作用下,可将CN-氧化成CNO-。CN-的电子式为_______,CNO-的中心原子的杂化方式为______。
(6)在CrCl3溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+ (n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
[CrCln(H2O)6-n]X++ xR- Rx[CrCln(H2O)6-n]+xH+。将含0.0015 mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol・L-1NaOH溶液25.00 mL,则该配离子的化学式为_______。
Rx[CrCln(H2O)6-n]+xH+。将含0.0015 mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol・L-1NaOH溶液25.00 mL,则该配离子的化学式为_______。
参考答案:(1)3 ?1s22s22p63s23p63d10?
(2)2 ? 8
(3)6 激发态的电子从能量高的轨道跃迁到能量较低的轨道时,以一定波长光的形式释放能量。
(4)BC?
(5)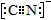 ?sp杂化?
?sp杂化?
(6)[CrCl(H2O)5]2+
本题解析:(1)第四周期中基态原子核外电子排布中4s轨道上只有1个电子的元素有K、Cr、Cu三种。Cu失去4s轨道上一个电子形成的Cu+核外电子排布为1s22s22p63s23p63d10。
(2)第四周期属于s区的元素是K、Ca两种。属于d区的元素是第IIIB族到第VIIB族及第VIII族,第四周期共有8种元素。
(3)根据晶胞结构示意图,可知Ca2+周围距Ca2+最近的O2-有6个,因此Ca2+的配位数为6。金属元素会有焰色反应,是因为激发态的电子从能量高的轨道跃迁到能量较低的轨道时,以一定波长光的形式释放能量。
(4)Na+半径小于K+半径,离子所带电荷相同时,半径越小晶格能越大,因此NaN3的晶格能高于KN3的晶格能,A错;K晶体为体心立方,每个晶胞中含有2个K原子,B正确;N原子的2p轨道半满,不容易失去电子,因此第一电离能N>O,C正确;氮气常温下稳定,因为氮气分子中含有氮氮三键,D错。
(5)CN-与N2是等电子体,因此电子式相似。CNO-与CO2是等电子体,因此中心原子杂化方式相同,是sp杂化。
(6)生成的H+的物质的量为:n(H+)=n(NaOH)=0.1200×25.00×10-3mol=0.003mol,根据方程式,可计算得出x=2。在配离子中,Cr+3价,根据化合价计算规则,可知n=1,则配离子为[CrCl(H2O)5]2+。
本题难度:一般
3、选择题 下列说法错误的是(?)
A.Na与Al为同周期元素,钠原子最外层有1个电子,铝原子最外层有3个电子,所以钠的金属性比铝强
B.Na与Mg为同周期元素,且Mg的核电荷数比Na的大,所以钠的金属性比镁强
C.NaOH为强碱,而Al(OH)3具有两性,所以钠的金属性比铝强
D.Zn+2Fe3+=Zn2++2Fe2+,所以Zn的金属性比Fe强
参考答案:D
本题解析:由反应Zn+Fe2+=Zn2++Fe才可说明Zn的金属性比Fe强。
本题难度:一般
4、填空题 五种短周期元素A、B、C、D、E的原子序数依次增大。A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。
回答下列问题:
(1)五种元素中,原子半径最大的是?,非金属性最强的是?(填元素符号)。
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是?(用化学式表示)。
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为?,其中存在的化学键类型为?。
(4)单质D在充足的单质E中燃烧,反应的化学方程式为?;
(5)单质E与水反应的离子方程式?。
参考答案:(1)Na? Cl
(2)PH3
(3)NH4Cl?离子键、共价键
(4)2P+5Cl2 2PCl5
2PCl5
(5)Cl2+H2O=H++ Cl-+HClO
本题解析:A和B形成的化合物在水中呈碱性,判断A是H元素,B是N元素;A和C同族,B和D同族,则C是Na元素,D是P元素;C和E形成的化合物在水中呈中性,则E是Cl元素,氯化钠的溶液呈中性。
(1)根据元素周期律判断,五种元素中,原子半径最大的是Na,非金属性最强的是Cl;
(2)B、D、E中非金属性最弱的是P,与H形成PH3的热稳定性最差;
(3)A和E形成的化合物是HCl,A和B形成的化合物是氨气,二者反应生成氯化铵化学式为NH4Cl,存在离子键、共价键;
(4)P在氯气中燃烧生成五氯化磷,化学方程式为2P+5Cl2 2PCl5
2PCl5
(5)氯气与水反应生成氯化氢和次氯酸,离子方程式为Cl2+H2O=H++ Cl-+HClO
本题难度:一般
5、选择题 已知金属元素X的+1价阳 离子最外层有2个电子,该阳离子有6个电子层。由此推知下列说法中正确的是( ?)
离子最外层有2个电子,该阳离子有6个电子层。由此推知下列说法中正确的是( ?)
A.X元素位于元素周期表的第六周期第ⅣA族
B.X元素的还原性比铝元素强
C.X(OH)3和Al(OH)3一样是两性氢氧化物
D.离子半径X3+ > X+
参考答案:B
本题解析:略
本题难度:一般