1、选择题 已知几种难溶电解质的溶度积常数(25℃)见下表

下列对AgCl、AgBr、AgI、Ag2SO4、Ag2CrO4叙述不正确的是
[? ]
A.Ksp的大小与三种卤化银见光分解的难易无关
B.将等体积的4×10-3 mol・L-1的AgNO3和4×10-3 mol・L-1 K2CrO4混合,有Ag2CrO4沉淀产生
C.向AgCl的悬浊液中滴加NaI的饱和溶液可以得到黄色AgI悬浊液
D.向100mL0.1mol・L-1的Na2SO4溶液中加入1mL0.1mol・L-1的AgNO3溶液,有白色沉淀生成
2、选择题 在溶液中有浓度均为0.01mol/L的Fe3+、Cr3+、Zn2+、Mg2+等离子,已知:Ksp[Fe(OH)3]=2.6×10-39; Ksp[Cr(OH)3] =7.0×10-31 Ksp[Zn(OH)2] =1.0×10-17; Ksp[Mg(OH)2] =1.8×10-11当氢氧化物开始沉淀时,下列哪一种离子所需溶液的pH最小
[? ]
A.Fe3+
B.Cr3+
C.Zn2+
D.Mg2+
3、选择题 自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜蓝(CuS)。下列分析正确的是?
[? ]
A.CuS的溶解度大于PbS的溶解度
B.原生铜的硫化物具有还原性,而铜蓝没有还原性
C.CuSO4与ZnS反应的离子方程式是Cu2+ + S2-=CuS↓
D.整个过程涉及的反应类型有氧化还原反应和复分解反应
4、填空题 活性ZnO在橡胶、塑料、涂料工业中有重要应用,一种由粗ZnO(含FeO、CuO)制备活性ZnO的流程如下(已知:碱式碳酸锌经焙烧可制得活性ZnO):
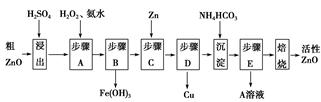
已知:几种离子生成氢氧化物沉淀时的pH如表:
待沉淀离子
| Fe2+
| Fe3+
| Zn2+
| Cu2+
|
开始沉淀时pH
| 6.34
| 1.48
| 6.2
| 5.2
|
完全沉淀时pH
| 9.7
| 3.2
| 8.0
| 6.4
|
?
请回答下列问题:
(1)步骤A加H2O2发生反应的离子方程式是?,该步骤需控制溶液pH的范围是?。
(2)A溶液中主要含有的溶质是?。
(3)碱式碳酸锌经焙烧制得活性ZnO的反应ΔH>0,该反应能自发进行的原因是ΔS?(选填“=”、“>”或“<”)0。
(4)若经处理后的废水pH=8,此时Zn2+的浓度为?mg/L(常温下,Ksp[Zn(OH)2]=1.2×10-17)。
5、选择题 下表提供的玻璃仪器(非玻璃仪器任选)及现象描述均符合相应实脸目的的是
选项
| 实验目的
| 玻璃仪器
| 实验现象
|
A
| 硫化锌沉淀转化为硫化铜沉淀
| 试管、胶头滴管
| 白色沉淀转化为黑色沉淀
|
B
| 验证CO2的氧化性
| 酒精灯、集气瓶、玻璃片
| 镁条剧烈燃烧,产生白色的烟雾,瓶内壁有白色粉末
|
C
| 分离乙酸乙酯与乙酸
| 分液漏斗、烧杯
| 液体分层,上层为无色油状液体,上层液体和下层液体都从分液漏斗下口放出
|
D
| 实验室制取乙烯
| 酒精灯、圆底烧瓶、导管
| 加热后液体沸腾,液体逐渐变黑,并有气体产生
|